O Brasil registrou 29.557 pedidos de patentes em 2025, o maior volume desde 2016, mas ainda carrega um passivo de mais de 115 mil processos pendentes no INPI. Para quem desenvolve dispositivos médicos, proteger a propriedade intelectual não é luxo acadêmico: é o que separa uma startup com poder de negociação de um projeto facilmente copiável. Com o mercado global de dispositivos médicos projetado para ultrapassar US$ 1 trilhão até 2034, entender as regras de patentes dispositivos médicos no sistema brasileiro é decisivo para captar investimento, licenciar tecnologia e competir internacionalmente.
Este artigo faz parte do Guia Definitivo de Engenharia Biomédica.
O Cenário de Patentes no Brasil: INPI em Números
O Instituto Nacional da Propriedade Industrial (INPI) é a autarquia federal responsável por conceder patentes, registrar marcas, contratos de transferência de tecnologia e desenhos industriais no Brasil. Nos últimos anos, o instituto passou por uma profunda reestruturação para reduzir o histórico backlog e acelerar o tempo de exame.
Indicadores recentes do INPI
| Indicador | Valor | Ano/Período |
|---|---|---|
| Pedidos de patente depositados | 29.557 | 2025 |
| Patentes concedidas | 13.624 | 2025 |
| Patentes concedidas (recorde) | 21.800 | 2022 |
| Backlog pendente | 115.000+ | 2025 |
| Tempo médio de exame | 2 a 10 anos | Varia por campo técnico |
| PPH, tempo médio | 6 meses | Fase V |
| PPH, taxa de aprovação | 95,94% | Fase V |
O pico de concessões em 2022 (21.800 patentes) resultou do Plano de Combate ao Backlog, que priorizou processos antigos. Desde então, o ritmo de concessão estabilizou em torno de 13-14 mil patentes anuais, enquanto os depósitos cresceram consistentemente. Para dispositivos médicos, a área técnica relevante é a Divisão de Patentes em Biotecnologia e Saúde, que costuma ter prazos na faixa superior (5 a 10 anos sem aceleração).
Em 2025, depositantes brasileiros representaram 26,2% dos pedidos no INPI, superando pela primeira vez os norte-americanos (23,5%) como principal pais de origem dos depositos de patentes.
— INPI, Relatorio Anual de Atividades, 2025
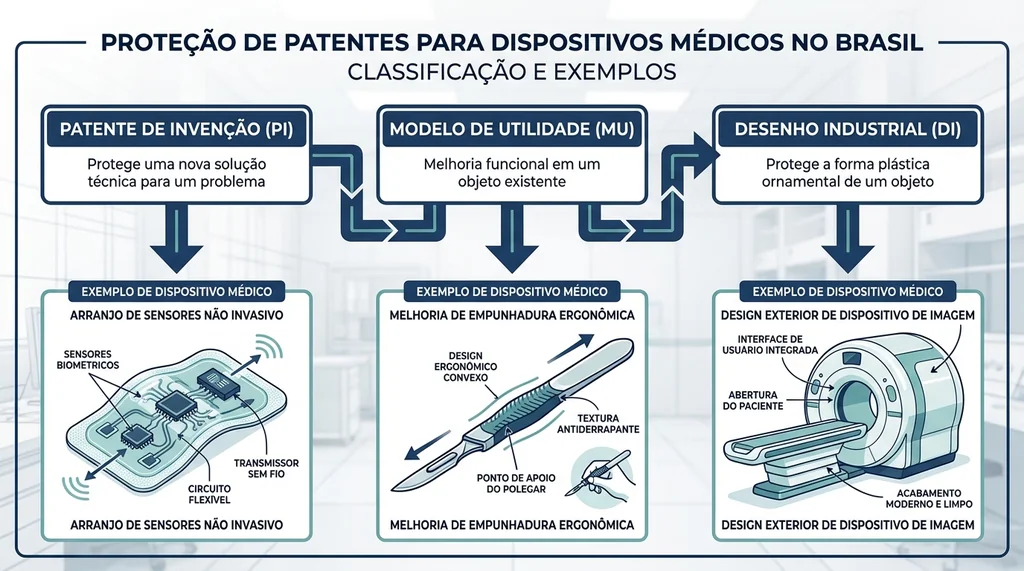
Descrição completa da imagem
Diagrama explicativo das modalidades de patente no Brasil para dispositivos médicos: Invenção, Utilidade e Desenho Industrial..
O que é patenteável em dispositivos médicos?
A Lei de Propriedade Industrial (Lei 9.279/1996) define três modalidades de proteção relevantes para o setor:
| Modalidade | Proteção | Prazo | Aplicação em Dispositivos Médicos |
|---|---|---|---|
| Patente de Invenção (PI) | Produto ou processo novo com atividade inventiva | 20 anos | Novo mecanismo de ação, sensor inovador, algoritmo com efeito técnico |
| Modelo de Utilidade (MU) | Melhoria funcional em objeto de uso prático | 15 anos | Aprimoramento ergonômico, adaptação de conector, redesign funcional |
| Desenho Industrial (DI) | Forma ornamental nova de objeto | Até 25 anos | Design externo de equipamento, interface visual de dispositivo |
É fundamental lembrar que o Brasil não permite patentes de métodos terapêuticos, cirúrgicos ou de diagnóstico praticados diretamente no corpo humano. Contudo, o dispositivo que executa esses métodos pode ser patenteado. Essa distinção é crítica para a redação de reivindicações: o foco deve estar no aparato técnico, não no procedimento clínico.
Custos e Prazos: Do Depósito à Concessão
Um dos maiores obstáculos para inventores independentes e pequenas empresas é o custo total do processo de patente. O INPI oferece, contudo, um sistema de descontos que pode reduzir significativamente o investimento inicial.
Tabela de custos INPI (2025/2026)
| Etapa | Valor Normal | Com Desconto (50%) |
|---|---|---|
| Depósito do pedido | R$ 260 | R$ 130 |
| Pedido de exame técnico | R$ 870 | R$ 435 |
| Anuidades (acumuladas ao longo do processo) | R$ 3.000 a R$ 8.000 | R$ 1.500 a R$ 4.000 |
| Honorários de agente de PI (estimativa) | R$ 8.000 a R$ 20.000 | N/A |
| Custo total estimado | R$ 15.000 a R$ 30.000 | R$ 8.000 a R$ 18.000 |
O desconto de 50% é aplicável a pessoas físicas, microempreendedores individuais (MEIs), microempresas (MEs), startups (conforme o Marco Legal das Startups), e instituições de ciência e tecnologia (ICTs). Para a maioria dos laboratórios universitários e spin-offs acadêmicas, esse desconto é automático mediante comprovação no momento do depósito.
Prazos realistas
Embora o INPI tenha feito avanços consideráveis, os prazos de exame ainda são longos para o setor de saúde. Na prática, um pedido de patente de dispositivo médico depositado sem qualquer aceleração pode levar de 5 a 10 anos até a decisão final. Fatores que influenciam esse prazo incluem: complexidade técnica do pedido, qualidade da busca de anterioridade, número de exigências formuladas pelo examinador e a carga de trabalho da divisão técnica responsável.
Existem, no entanto, mecanismos para acelerar esse processo significativamente, como o PPH e o Exame Prioritário.
PPH: Acelerando a Concessão com Acordos Internacionais
O Patent Prosecution Highway (PPH) é um dos instrumentos mais poderosos disponíveis para inventores de dispositivos médicos que buscam proteção simultânea no Brasil e em outros mercados. Funciona assim: se o depositante já obteve parecer favorável (ou concessão) em um escritório parceiro, pode solicitar exame acelerado no INPI com base nesse resultado.
Dados do PPH no Brasil, Fase V
- Tempo médio de decisão: 6 meses (comparado a 5-10 anos no fluxo normal)
- Taxa de aprovação: 95,94% dos pedidos PPH resultam em concessão
- Cota anual: 3.200 pedidos por ano
- Escritórios parceiros: USPTO (EUA), EPO (Europa), JPO (Japão), KIPO (Coreia), entre outros
Para fabricantes de dispositivos médicos com estratégia global, o fluxo ideal é: depositar primeiro no escritório com exame mais rápido (tipicamente USPTO ou JPO), obter o parecer favorável e então acionar o PPH no INPI. O resultado é uma redução de anos para meses no tempo de concessão brasileiro, com taxa de sucesso próxima de 96%.
Exame prioritário
Além do PPH, o INPI oferece exame prioritário em situações específicas: depositantes com 60 anos ou mais, portadores de deficiência ou doença grave, instituições de ciência e tecnologia, e pedidos relacionados a programas governamentais (como o Plano Nacional de Saúde). Para startups de saúde, o enquadramento como ICT ou a vinculação a programas de aceleração pública pode abrir essa via.
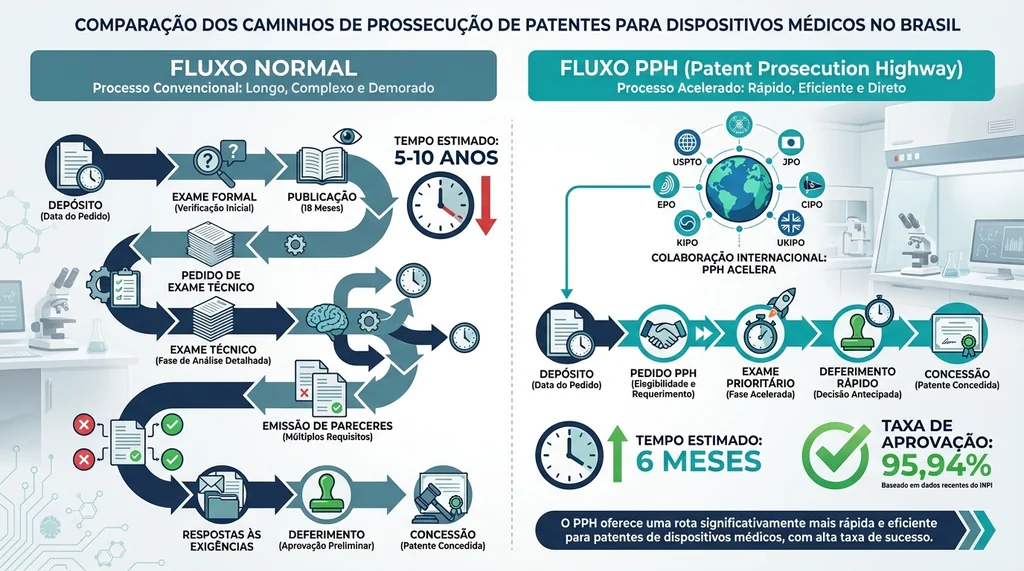
Descrição completa da imagem
Infográfico comparando o tempo de concessão de patentes para dispositivos médicos: Fluxo Normal (5-10 anos) vs. PPH (6 meses)..
Proteção Internacional: O Sistema PCT
Para quem pretende comercializar dispositivos médicos fora do Brasil, ou atrair investidores internacionais que valorizam portfólio global de PI, o Tratado de Cooperação em Matéria de Patentes (PCT) é o caminho mais eficiente. Administrado pela OMPI/WIPO o PCT permite que um único depósito internacional sirva de base para proteção em mais de 150 países.
Fluxo PCT para dispositivos médicos
- Depósito internacional: pedido único via INPI (como escritório receptor) ou diretamente na OMPI
- Busca internacional: relatório de busca e opinião preliminar emitidos por uma Autoridade de Busca Internacional (ISA)
- Publicação internacional: 18 meses após a data de prioridade
- Fase nacional: o depositante tem até 30 meses da data de prioridade para ingressar nos países de interesse
Custos estimados do PCT
| Fase | Custo Estimado |
|---|---|
| Fase internacional (depósito + busca) | USD 3.000 a USD 5.000 |
| Fase nacional (por país, média) | USD 2.000 a USD 8.000 |
| Tradução (por país) | USD 1.000 a USD 3.000 |
| Honorários locais (por país) | USD 1.500 a USD 5.000 |
O grande benefício do PCT é o prazo de 30 meses para decidir em quais países investir. Para uma startup de dispositivo médico que ainda está validando produto e mercado, isso significa ganhar tempo para captar investimento antes de arcar com os custos da fase nacional. Os países prioritários para dispositivos médicos geralmente são EUA, Europa (via EPO), Japão e China, que juntos representam mais de 70% do mercado global.
Patentes de Software Médico e Inteligência Artificial
A patenteabilidade de software e algoritmos de IA aplicados à saúde é um dos temas mais dinâmicos na propriedade intelectual de dispositivos médicos. No Brasil, o INPI tem evoluído suas diretrizes para acompanhar essa transformação tecnológica, mantendo a premissa de que invenções implementadas por computador são patenteáveis quando produzem efeito técnico concreto.
Marco normativo para SaMD e IA
- Portaria INPI 411/2020: estabelece as diretrizes para exame de invenções implementadas por computador, confirmando que software com efeito técnico pode ser patenteado
- Portaria INPI/DIRPA 16/2024: define três categorias de invenções envolvendo inteligência artificial para fins de classificação e exame de patentes
- RDC 657/2022 (ANVISA): regulamenta Software como Dispositivo Médico (SaMD) incluindo aqueles baseados em IA
As três categorias definidas pela Portaria 16/2024 para invenções de IA são: (1) IA como ferramenta no processo inventivo, (2) IA como componente da invenção, e (3) métodos de treinamento e arquiteturas de IA com efeito técnico. Para dispositivos médicos baseados em IA, como algoritmos de diagnóstico por imagem ou sistemas de apoio à decisão clínica, a categoria mais relevante é a segunda, onde o modelo de IA é parte integral do dispositivo e contribui para o efeito técnico reivindicado.
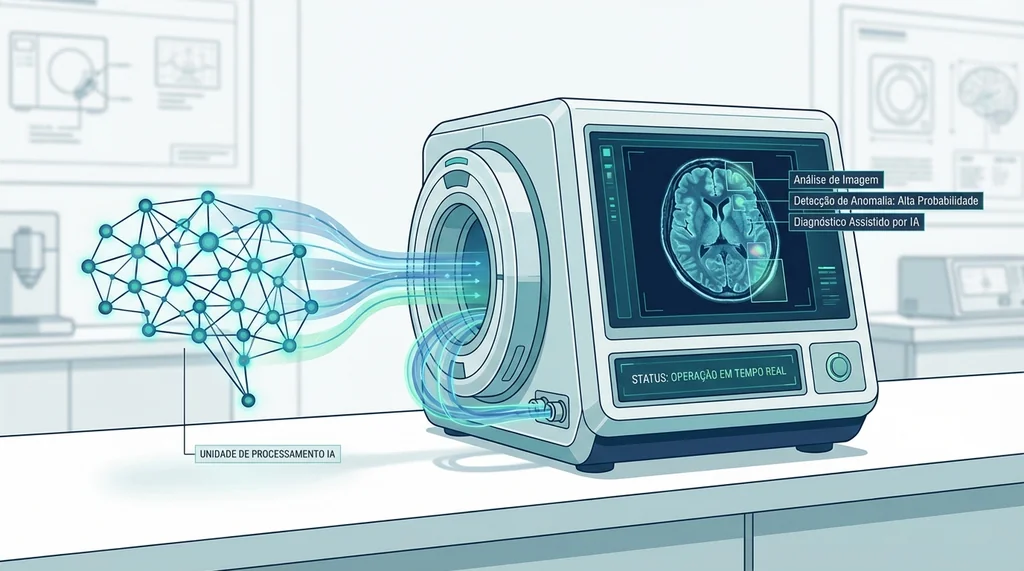
Estratégias de redação para software médico
A redação de reivindicações para SaMD requer cuidados específicos para evitar a rejeição por se enquadrar como "programa de computador em si" (excluído pela Lei 9.279/1996). As melhores práticas incluem:
- Focar no efeito técnico: descrever o resultado concreto que o software produz (ex.: detecção de arritmia com sensibilidade de X%), não apenas o algoritmo abstrato
- Incluir reivindicações de sistema: combinar hardware e software em um único dispositivo (ex.: "sistema de monitoramento cardíaco compreendendo sensor, processador e módulo de IA configurado para...")
- Documentar dados de validação clínica: relatórios de ensaios clínicos ou estudos de desempenho reforçam o caráter técnico da invenção
- Referenciar standards relevantes: ISO 13485 IEC 62304 (ciclo de vida de software médico) e IEC 82304
ANVISA e INPI: processos independentes
Uma dúvida recorrente entre inventores de dispositivos médicos é a relação entre o registro sanitário na ANVISA e a concessão de patente pelo INPI. Diferentemente do setor farmacêutico, onde existe o mecanismo de anuência prévia da ANVISA para patentes de medicamentos, para dispositivos médicos os dois processos são completamente independentes.
Isso significa que:
- O registro ANVISA não depende de ter patente concedida
- A concessão de patente pelo INPI não depende de aprovação ANVISA
- Os dois processos podem (e devem) tramitar em paralelo
- Não há linkage farmacêutico para dispositivos médicos
Na prática, a estratégia ideal para fabricantes é iniciar ambos os processos simultaneamente: depositar a patente no INPI assim que a invenção estiver suficientemente descrita, e iniciar a documentação regulatória para a ANVISA conforme o produto avança no desenvolvimento. Lembre-se de que a publicação do pedido de patente ocorre 18 meses após o depósito, enquanto o registro ANVISA pode ser obtido em prazos variáveis dependendo da classe de risco do dispositivo.
Incentivos Fiscais e Transferência de Tecnologia
Além da proteção conferida pela patente em si, o sistema brasileiro oferece incentivos fiscais significativos para empresas que investem em P&D e obtêm patentes. O principal mecanismo é a Lei do Bem (Lei 11.196/2005), que permite:
- Exclusão de 60% dos gastos com P&D da base de cálculo do IRPJ e CSLL
- Adicional de 20% quando há concessão de patente (elevando a exclusão total para 80%)
- Depreciação acelerada integral de equipamentos de pesquisa
- Redução de 50% do IPI sobre equipamentos e instrumentos de pesquisa
Para uma empresa de dispositivos médicos que investe R$ 2 milhões anuais em P&D e obtém uma patente, o benefício fiscal combinado da Lei do Bem pode representar uma economia de R$ 500 mil a R$ 700 mil ao ano. Esse incentivo é particularmente relevante para fabricantes nacionais que competem com importados e precisam amortizar o investimento em inovação.
Em 2022, 3.493 empresas investiram R$ 35,74 bilhoes em P&D via Lei do Bem, com renuncia fiscal de R$ 7,9 bilhoes. A lei preve adicional de 20% na exclusao tributaria quando ha concessao de patente.
— MCTI / Relatorio Anual da Lei do Bem, 2022
Transferência de tecnologia e NITs
Os Núcleos de Inovação Tecnológica (NITs) são estruturas obrigatórias em universidades e ICTs públicas desde a Lei de Inovação (Lei 10.973/2004). Eles são responsáveis por gerir a propriedade intelectual gerada nas instituições e facilitar a transferência de tecnologia para o setor produtivo.
Os dados mais recentes mostram, contudo, um cenário desafiador: apenas 23,8% dos NITs assinaram novos contratos de licenciamento em 2023. Isso indica uma lacuna significativa entre a produção de patentes nas universidades e a efetiva transferência dessas tecnologias para empresas que podem transformá-las em produtos no mercado. Para entender as etapas envolvidas nessa jornada, consulte nosso artigo sobre o caminho do laboratório ao mercado na pesquisa de produtos médicos.
Existem exceções notáveis. A Inova Unicamp, agência de inovação da Universidade Estadual de Campinas, mantém 212 contratos ativos de transferência de tecnologia, sendo referência nacional em interação universidade-empresa. Para dispositivos médicos, centros como o CEB/UNICAMP e o PEB/COPPE/UFRJ possuem portfólios de patentes com potencial comercial significativo em áreas como processamento de imagens médicas, instrumentação biomédica e biomateriais.
A EMBRAPII investiu R$ 252 milhoes em 263 projetos de saude, gerando 95 pedidos de propriedade intelectual. O INPI instalou centros de PI em 7 Unidades EMBRAPII e o programa de Telementoria capacita 70 profissionais em 32 unidades.
— EMBRAPII / INPI, 2024
Casos Brasileiros: Da Patente ao Mercado Global
O ecossistema brasileiro de dispositivos médicos já produziu casos emblemáticos de empresas que transformaram propriedade intelectual em vantagem competitiva global. Esses exemplos demonstram que a combinação de inovação técnica, proteção patentária e estratégia regulatória pode levar tecnologias brasileiras ao mercado internacional.
brain4care
A brain4care, startup originada na USP São Carlos, desenvolveu um sensor não invasivo de pressão intracraniana, uma tecnologia que historicamente exigia procedimento neurocirúrgico invasivo. Com portfólio de patentes protegendo o método de medição e o dispositivo, a empresa obteve a aprovação FDA via pathway 510(k), abrindo o mercado norte-americano. O caso ilustra como a proteção de PI desde a fase acadêmica pode sustentar uma trajetória de internacionalização.
Magnamed
A Magnamed, fabricante brasileira de ventiladores pulmonares, consolidou-se como referência em ventilação mecânica e anestesia. Com um portfólio robusto de propriedade intelectual e certificações internacionais, a empresa conquistou um contrato de R$ 322,5 milhões e exporta para mais de 40 países. A proteção patentária foi decisiva para negociar acordos de fornecimento governamentais e licenciamentos internacionais, além de atrair investidores de impacto.
Fanem e Nanox
A Fanem com mais de 90 anos de atuação, é a maior fabricante brasileira de incubadoras neonatais e equipamentos para cuidados neonatais, com presença em mais de 100 países. Seu portfólio de patentes protege inovações incrementais em controle térmico e fototerapia. A Nanox por sua vez, é uma empresa de nanobiotecnologia que desenvolveu biomateriais antimicrobianos para revestimento de dispositivos médicos, com patentes em nanopartículas de prata e óxido de zinco com aplicações em cateteres e implantes.
Esses casos têm em comum a construção precoce de portfólios de PI, o uso estratégico do sistema PCT para proteção internacional e a integração entre estratégia patentária e estratégia regulatória (ANVISA + FDA/CE).
Perguntas Frequentes
Quanto tempo leva para obter uma patente de dispositivo médico no Brasil?
No fluxo normal do INPI, o exame de patentes na área de saúde pode levar de 5 a 10 anos. Contudo, utilizando o Patent Prosecution Highway (PPH), esse prazo cai para aproximadamente 6 meses, com taxa de aprovação de 95,94%. O exame prioritário também está disponível para ICTs e pedidos vinculados a programas governamentais de saúde. A chave é planejar a estratégia de aceleração desde o momento do depósito.
Qual é o custo total para patentear um dispositivo médico no Brasil?
O custo total estimado varia de R$ 15.000 a R$ 30.000, incluindo taxas do INPI (depósito de R$ 260, exame de R$ 870, anuidades acumuladas) e honorários de agente de propriedade industrial. Pessoas físicas, MEIs, microempresas, startups e ICTs têm direito a desconto de 50% em todas as taxas oficiais, o que pode reduzir o custo total para a faixa de R$ 8.000 a R$ 18.000.
Software médico (SaMD) pode ser patenteado no Brasil?
Sim. A Portaria INPI 411/2020 confirma que invenções implementadas por computador são patenteáveis quando produzem efeito técnico concreto. Para softwares médicos, isso significa que algoritmos de diagnóstico, sistemas de monitoramento baseados em IA e plataformas de apoio à decisão clínica podem ser protegidos por patente de invenção, desde que as reivindicações focalizem o efeito técnico e não o programa de computador em si.
Preciso ter registro na ANVISA para depositar uma patente de dispositivo médico?
Não. Os processos no INPI e na ANVISA são completamente independentes para dispositivos médicos. Não existe anuência prévia nem linkage como ocorre com medicamentos. A recomendação é iniciar ambos os processos em paralelo: o depósito de patente assim que a invenção estiver descrita e a documentação regulatória conforme o produto avança no desenvolvimento.
Como funciona a proteção internacional de patentes via PCT?
O sistema PCT permite depositar um único pedido internacional que serve de base para proteção em mais de 150 países. O custo da fase internacional é de USD 3.000 a USD 5.000, e o depositante tem 30 meses da data de prioridade para decidir em quais países entrar na fase nacional. Para dispositivos médicos, os mercados prioritários geralmente são EUA (USPTO), Europa (EPO), Japão (JPO) e China (CNIPA).
A proteção de propriedade intelectual é um pilar estratégico para o desenvolvimento do setor de dispositivos médicos no Brasil. Com mecanismos como o PPH, incentivos da Lei do Bem e um marco normativo cada vez mais claro para SaMD e IA, o país oferece ferramentas concretas para que inventores e empresas protejam suas inovações e acessem mercados globais. Para artigos relacionados, consulte: ANVISA e Dispositivos Médicos, Guia de Regulamentação SaMD, Software como Dispositivo Médico Mercado de Dispositivos Médicos no Brasil e Financiamento para Inovação em Saúde. Fontes oficiais: INPI, Instituto Nacional da Propriedade Industrial OMPI/WIPO, Tratado PCT ANVISA, Agência Nacional de Vigilância Sanitária ABIMO, Associação Brasileira da Indústria de Artigos e Equipamentos Médicos e MCTI, Ministério da Ciência, Tecnologia e Inovação.
Conteúdo elaborado pela equipe editorial do Guia Definitivo de Engenharia Biomédica com base nas publicações oficiais do INPI, OMPI e legislação brasileira de propriedade industrial. Atualizado em fevereiro de 2026.
Artigos relacionados
Biomateriais: Dos Implantes de Titânio à Bioimpressão 3D [2026]
Guia técnico-científico completo sobre biomateriais na engenharia biomédica: classificação, biocompatibilidade, aplicações clínicas, empresas brasileiras, bioimpressão 3D e mercado global de USD 48 bilhões.
Biomecânica na Engenharia Biomédica [2026]: FEA, Próteses e Análise de Movimento
Guia técnico completo sobre biomecânica na engenharia biomédica: propriedades mecânicas de tecidos, análise de movimento por captura óptica e IA, pipeline de elementos finitos (FEA), design de próteses, implantes ortopédicos, biomecânica cardiovascular e as principais tendências de 2026.
Centros de Pesquisa em Engenharia Biomedica: Mapa Completo do Brasil [2026]
Guia atualizado com mais de 50 centros de pesquisa em engenharia biomedica em 13 estados brasileiros. Conheca os programas com nota CAPES 6 e 7, laboratorios de referencia, linhas de pesquisa, financiamento e como ingressar na pos-graduacao.
Como Publicar Artigos Cientificos em Engenharia Biomedica: Guia Completo [2026]
Guia pratico para publicar artigos cientificos em Engenharia Biomedica: escolha de revistas (Nature BME, IEEE, RBEB), metricas de impacto (JIF, CiteScore, h-index), acesso aberto via CAPES, custos de APC e estrategias para aumentar suas chances de aceite em 2026.