Transformar uma descoberta de laboratorio em um produto medico comercializado no Brasil leva, em media, de 7 a 15 anos e exige investimentos que frequentemente ultrapassam R$ 200 mil apenas em custos regulatorios. A jornada envolve desafios tecnologicos, regulatorios e empresariais que a formacao academica tradicional nao cobre, e apenas 3,5% das patentes universitarias brasileiras chegam efetivamente ao setor produtivo. Para engenheiros biomedicos, pesquisadores e empreendedores, compreender cada etapa dessa travessia e o que separa um paper publicado de um produto que salva vidas.
Este artigo faz parte do Guia Definitivo de Engenharia Biomedica.
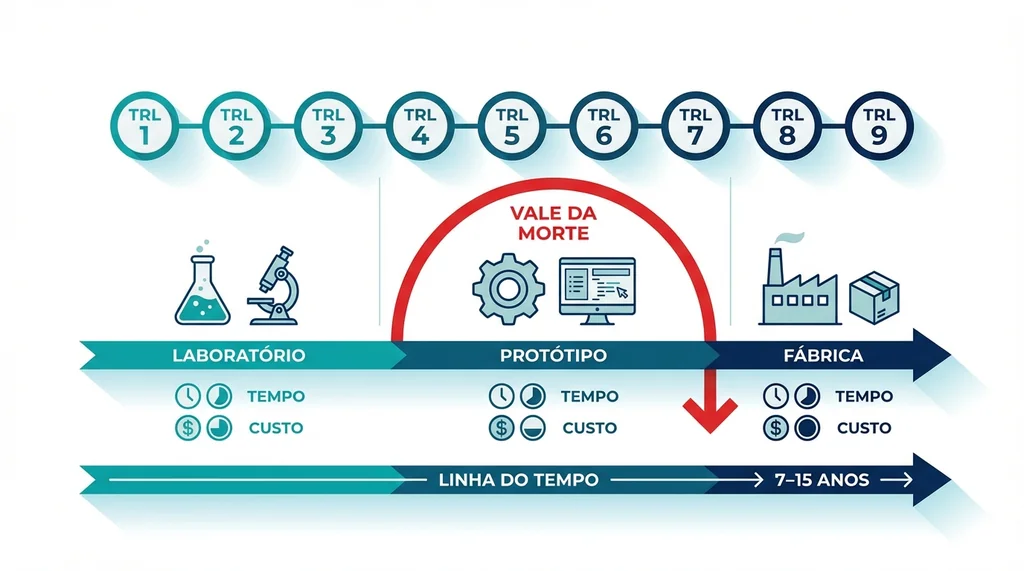
O Vale da Morte entre Pesquisa e Mercado
O conceito de "vale da morte" descreve a fase critica em que uma tecnologia ja demonstrou viabilidade cientifica, mas ainda nao tem maturidade suficiente para atrair investimento privado. No setor de dispositivos medicos, esse vale e particularmente profundo: alem das barreiras tecnicas comuns a qualquer inovacao, existem exigencias regulatorias rigorosas, ensaios clinicos obrigatorios e uma cadeia de certificacoes que multiplicam o tempo e o custo de desenvolvimento.
Os numeros brasileiros ilustram a dimensao do problema. Segundo o Formulario para Informacoes sobre a Politica de Propriedade Intelectual (FORMICT/MCTI), apenas 23,8% dos 130 Nucleos de Inovacao Tecnologica (NITs) ativos em universidades brasileiras firmaram novos contratos de licenciamento em 2023. Quando se olha para patentes, o cenario e ainda mais restrito: somente 3,5% das patentes universitarias foram efetivamente transferidas para o setor produtivo.
O Brasil produz apenas 45% do que consome em produtos de saude, gerando um deficit comercial de US$ 8,62 bilhoes. Ao mesmo tempo, o pais ja abriga mais de 1.200 healthtechs ativas e exportou US$ 1,17 bilhao em dispositivos medicos em 2024. Esses dados revelam uma assimetria: ha capacidade instalada de pesquisa e um mercado consumidor gigantesco, mas a ponte entre os dois permanece fragil.
Apenas 3,5% das patentes universitarias brasileiras foram efetivamente transferidas para o setor produtivo na ultima decada, e a receita com licenciamentos ativos nos NITs caiu de R$ 48 milhoes em 2021 para R$ 32 milhoes em 2023.
— Pesquisa FORTEC de Inovacao / FORMICT-MCTI, 2023
Por que projetos morrem no vale da morte
Tres fatores principais explicam a alta mortalidade de projetos em transicao:
- Gap de competencias: pesquisadores dominam a ciencia, mas frequentemente carecem de habilidades em gestao, regulatorio e comercializacao. A formacao academica brasileira privilegia publicacoes sobre transferencia tecnologica
- Descontinuidade de financiamento: agencias de fomento financiam pesquisa basica (TRL 1-3) e, em menor grau, prova de conceito (TRL 4-5), mas ha um vazio critico entre TRL 5 e TRL 7, quando o prototipo precisa ser validado clinicamente e adequado regulatoriamente
- Tempo regulatorio: o registro de dispositivos Classe III ou IV na ANVISA pode levar de 12 a 24 meses, periodo durante o qual o projeto consome recursos sem gerar receita
Niveis de Maturidade Tecnologica (TRL): O Roteiro da Translacao
A escala TRL (Technology Readiness Level), padronizada pela ABNT NBR ISO 16290:2015, fornece uma linguagem comum para avaliar o estagio de desenvolvimento de uma tecnologia. Para dispositivos medicos, a jornada do TRL 1 ao TRL 9 envolve etapas especificas que vao alem do desenvolvimento tecnico puro:
| TRL | Descricao | Marco para Dispositivos Medicos | Financiamento Tipico |
|---|---|---|---|
| 1-2 | Principios basicos observados e formulados | Publicacao cientifica, revisao de literatura de patentes | CNPq, FAPESP (bolsas) |
| 3 | Prova de conceito experimental | Testes in vitro, simulacoes, modelo computacional | FAPESP PIPE Fase 1, editais tematicos |
| 4 | Validacao em ambiente de laboratorio | Prototipo funcional, testes de biocompatibilidade iniciais | EMBRAPII, FINEP subvencao |
| 5 | Validacao em ambiente relevante | Testes pre-clinicos, dossiê tecnico preliminar | FAPESP PIPE Fase 2, FINEP |
| 6 | Demonstracao em ambiente relevante | Ensaio clinico piloto, adequacao a normas (IEC 60601, ISO 13485) | FINEP, investidores anjo |
| 7 | Demonstracao em ambiente operacional | Ensaio clinico completo, submissao a ANVISA | Venture capital, BNDES |
| 8 | Sistema qualificado e completo | Registro ANVISA obtido, producao piloto, certificacao INMETRO | BNDES, investimento privado |
| 9 | Sistema operacional em ambiente real | Comercializacao ativa, tecnovigilancia pos-mercado | Receita propria, credito comercial |
Um erro comum e subestimar os requisitos de cada transicao. A passagem do TRL 3 para o TRL 4, por exemplo, exige que o pesquisador comece a pensar em propriedade intelectual, liberdade de operacao (freedom to operate) e viabilidade de manufatura, questoes que raramente aparecem em projetos de pesquisa academica tradicionais.
Marco Legal de CT&I: O Que Mudou com a Lei 13.243/2016
O Marco Legal da Ciencia, Tecnologia e Inovacao (Lei 13.243/2016) representou um avanco significativo para a transferencia tecnologica no Brasil. Entre as mudancas mais relevantes para o setor de dispositivos medicos:
- Flexibilizacao da dedicacao exclusiva: pesquisadores em regime de dedicacao exclusiva podem participar de atividades em empresas de base tecnologica, incluindo spin-offs originadas de suas pesquisas
- Compartilhamento de laboratorios: universidades podem compartilhar infraestrutura e equipamentos com empresas mediante contratos simplificados, eliminando a necessidade de licitacao em muitos casos
- NITs com maior autonomia: os Nucleos de Inovacao Tecnologica ganharam a possibilidade de operar como fundacoes de apoio, agilizando processos de licenciamento e transferencia
- Encomenda tecnologica: o poder publico pode contratar diretamente ICTs e empresas para desenvolver solucoes para problemas especificos do SUS, sem necessidade de licitacao convencional
Na pratica, o Marco Legal reduziu barreiras burocraticas, mas sua implementacao permanece desigual. Universidades com NITs mais estruturados, como USP, UNICAMP e UFMG, conseguem operacionalizar as novas regras com mais eficiencia, enquanto instituicoes menores ainda enfrentam dificuldades na regulamentacao interna dos dispositivos da lei.
Propriedade intelectual: patentear ou publicar?
Essa e a primeira decisao estrategica que um pesquisador enfrenta. A publicacao cientifica gera reconhecimento academico, mas pode inviabilizar o deposito de patente posterior, no Brasil, o prazo de graca e de 12 meses apos a divulgacao publica. A recomendacao para projetos com potencial de transferencia e clara: depositar o pedido de patente antes de submeter o artigo.
O custo de deposito de patente no INPI para pessoa fisica ou microempresa e relativamente acessivel (cerca de R$ 175 para deposito + R$ 590 para exame), mas o processo de obtencao pode levar de 5 a 8 anos. Para protecao internacional via PCT (Patent Cooperation Treaty), os custos sobem para R$ 20.000-50.000 considerando traducoes e taxas de escritorios estrangeiros.
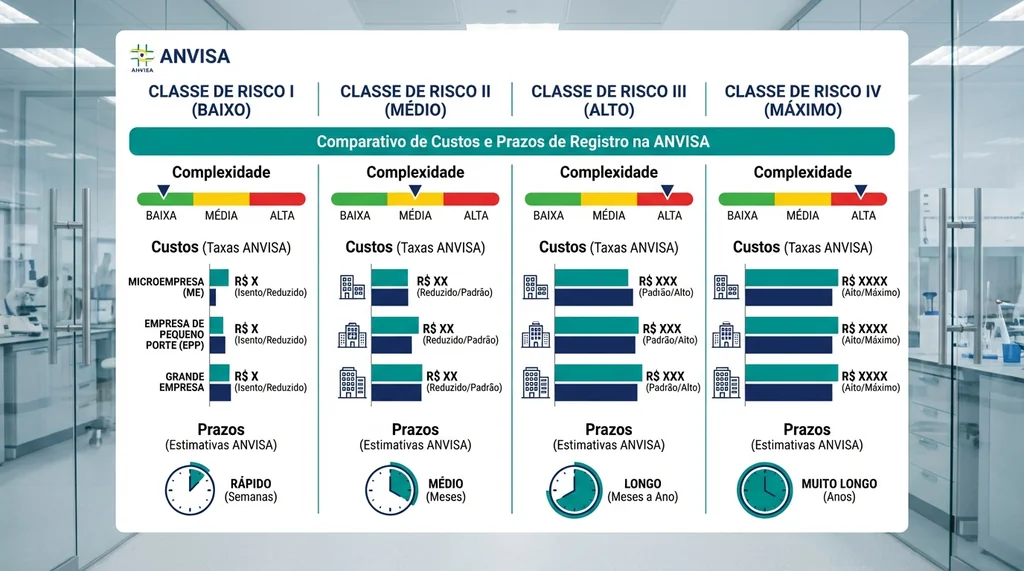
Registro ANVISA: Custos, Prazos e Classes de Risco
A RDC 751/2022 estabeleceu o framework regulatorio vigente para dispositivos medicos no Brasil, alinhado ao sistema IMDRF (International Medical Device Regulators Forum) com quatro classes de risco:
| Classe | Risco | Exemplos | Via de Registro | Prazo Medio |
|---|---|---|---|---|
| I | Baixo | Afastadores cirurgicos, algodao, luvas | Notificacao | 30-60 dias |
| II | Medio-baixo | Agulhas, cateteres simples, estetoscopios | Registro simplificado | 3-6 meses |
| III | Medio-alto | Ventiladores, monitores multiparametro, implantes ortopedicos | Registro completo | 12-18 meses |
| IV | Alto | Stents, marcapassos, dispositivos implantaveis ativos | Registro completo + parecer tecnico especial | 18-24 meses |
Custos de registro por porte de empresa
A ANVISA pratica valores diferenciados conforme o porte do fabricante, o que impacta diretamente a viabilidade financeira de spin-offs academicas:
| Porte da Empresa | Taxa de Registro (Classe I/II) | Taxa de Registro (Classe III/IV) |
|---|---|---|
| Microempresa (ME) | R$ 4.400 | R$ 5.000 |
| Empresa de Pequeno Porte (EPP) | R$ 11.000 | R$ 25.000 |
| Media empresa | R$ 44.000 | R$ 55.000 |
| Grande empresa | R$ 88.000 | R$ 108.000+ |
Alem das taxas da ANVISA, o orcamento regulatorio deve incluir a certificacao ISO 13485 (Sistema de Gestao da Qualidade para dispositivos medicos), que custa entre R$ 17.000 e R$ 45.000 dependendo do escopo e do organismo certificador. Para dispositivos eletromedicos, a certificacao de conformidade com a serie IEC 60601 junto ao INMETRO adiciona mais R$ 15.000-40.000 ao orcamento.
No total, uma spin-off de pequeno porte que desenvolve um dispositivo Classe III deve prever entre R$ 80.000 e R$ 200.000 apenas em custos regulatorios diretos, sem contar ensaios clinicos, que podem adicionar R$ 100.000-500.000 dependendo da complexidade.
Criando uma Spin-off Biomedica: Estrutura e Estrategia
A criacao de uma spin-off academica e o caminho mais comum para transferir tecnologia do laboratorio ao mercado no setor de dispositivos medicos. O modelo funciona porque permite que a propriedade intelectual gerada na universidade seja licenciada para uma empresa dedicada exclusivamente a desenvolve-la comercialmente.
Passos para criar uma spin-off biomedica
- Mapeamento de PI: identificar todas as patentes, know-how e segredos industriais associados a tecnologia. Realizar busca de anterioridade e analise de liberdade de operacao
- Negociacao com o NIT: formalizar contrato de licenciamento com a universidade. Os termos tipicos incluem royalties de 1-5% sobre receita liquida, pagamentos minimos anuais e clausulas de desempenho (milestones)
- Constituicao juridica: definir tipo societario (LTDA ou S/A), acordo de socios, vesting para fundadores e estrutura de governanca. Para spin-offs academicas, e comum iniciar como microempresa (ME) para aproveitar as taxas reduzidas da ANVISA
- Plano regulatorio: mapear todas as certificacoes, ensaios e registros necessarios antes de investir em desenvolvimento de produto. A estrategia regulatoria define o orcamento e o cronograma
- Captacao de recursos: combinar financiamento publico (PIPE, EMBRAPII, subvencao FINEP) com capital privado (anjos, venture capital) conforme o TRL do projeto
Modelo de negocios para dispositivos medicos
Diferentemente de software, dispositivos medicos fisicos exigem manufatura, logistica e assistencia tecnica. Os modelos mais adotados por spin-offs brasileiras incluem:
- Venda direta ao SUS: via licitacao ou pregao eletronico. Exige registro ANVISA ativo e inscricao no Comprasnet. O SUS e o maior comprador individual de dispositivos medicos no Brasil
- Venda para rede privada: via distribuidores especializados ou forca comercial propria. Hospitais privados valorizam inovacao e podem ser early adopters
- Modelo de comodato + insumos: o equipamento e cedido em comodato e a receita vem dos insumos consumiveis. Comum em diagnostico in vitro
- Licenciamento da tecnologia: para startups que nao desejam fabricar, licenciar para um fabricante estabelecido reduz risco operacional e acelera o acesso ao mercado
Ecossistema de Apoio: Incubadoras, Aceleradoras e Programas
O Brasil desenvolveu um ecossistema robusto de apoio a transferencia tecnologica em saude, com destaque para tres modelos complementares: incubadoras hospitalares, programas de financiamento publico e parques tecnologicos.
Incubadoras hospitalares de referencia
| Incubadora | Instituicao | Foco | Diferencial |
|---|---|---|---|
| Eretz.bio | Hospital Israelita Albert Einstein | Healthtechs com potencial de impacto clinico | Acesso direto a corpo clinico e infraestrutura hospitalar para validacao |
| InovaHC | HC-FMUSP | Solucoes para o SUS e hospitais publicos | Maior hospital publico da America Latina como campo de teste |
| Supera | USP Ribeirao Preto | Dispositivos medicos e biotecnologia | Parque tecnologico integrado com laboratorios da USP |
Essas incubadoras oferecem algo que aceleradoras genericas nao conseguem: acesso a ambiente clinico real para validacao de tecnologias. Uma startup incubada na Eretz.bio, por exemplo, pode testar seu dispositivo em ambiente hospitalar com acompanhamento de medicos e enfermeiros, gerando dados clinicos valiosos para o registro na ANVISA.
EMBRAPII: o modelo tripartite
A Empresa Brasileira de Pesquisa e Inovacao Industrial (EMBRAPII) opera um modelo de financiamento nao reembolsavel em que os custos de P&D sao divididos em tres partes iguais: 1/3 EMBRAPII, 1/3 unidade de pesquisa credenciada e 1/3 empresa. Para dispositivos medicos, as unidades EMBRAPII mais relevantes incluem o CTI Renato Archer (Campinas), o SENAI CIMATEC (Salvador) e o IPT (Sao Paulo).
O diferencial do modelo EMBRAPII e a agilidade: nao ha editais. A empresa negocia diretamente com a unidade credenciada, define o escopo do projeto e inicia a execucao em semanas, nao meses. O aporte medio por projeto e de R$ 500.000-2.000.000, cobrindo desenvolvimento de prototipo, testes de validacao e adequacao a normas tecnicas.
A EMBRAPII ja financiou aproximadamente 300 projetos e R$ 315 milhoes em P&D&I em saude, sendo o segundo maior setor do seu portfolio. Em 2025, anunciou um pacote de R$ 150 milhoes para projetos de alto impacto em dispositivos medicos e diagnosticos avancados.
— EMBRAPII, 2025
FAPESP PIPE: financiamento para empresas de base tecnologica
O Programa de Pesquisa Inovativa em Pequenas Empresas (PIPE) da FAPESP e um dos instrumentos mais eficazes para spin-offs academicas em Sao Paulo. Dividido em tres fases, o programa financia desde a prova de conceito (Fase 1, ate R$ 250.000 em 9 meses) ate o desenvolvimento de produto comercializavel (Fase 2, ate R$ 1.000.000 em 24 meses).
Para healthtechs, o PIPE tem um historico expressivo: diversas empresas que hoje lideram o mercado de dispositivos medicos no Brasil iniciaram sua trajetoria com financiamento PIPE, incluindo a Magnamed (ventiladores pulmonares) e a Timpel (tomografia por impedancia eletrica).
Cases de Sucesso: Da Pesquisa ao Produto
Tres cases brasileiros ilustram caminhos distintos de transferencia tecnologica em dispositivos medicos:
brain4care: do laboratorio da USP ao FDA
A brain4care desenvolveu um sensor nao invasivo para monitoramento da pressao intracraniana, tecnologia originada em pesquisa academica na Escola de Engenharia de Sao Carlos (USP). A empresa obteve a aprovacao FDA 510(k) nos Estados Unidos, demonstrando que e possivel percorrer a jornada completa, da pesquisa academica brasileira ao mercado regulado mais exigente do mundo. O caso brain4care destaca a importancia de uma estrategia regulatoria internacional desde o inicio: a empresa planejou simultaneamente o registro ANVISA e a submissao ao FDA.
Magnamed: ventiladores made in Brazil
A Magnamed, fundada em 2003, tornou-se uma das principais fabricantes de ventiladores pulmonares do Brasil. Durante a pandemia de COVID-19, a empresa escalou sua producao de forma dramatica para atender a demanda emergencial do SUS. Iniciada com financiamento FAPESP PIPE e FINEP, a Magnamed demonstra como a combinacao de financiamento publico em fases iniciais e competencia tecnica em engenharia biomedica pode gerar uma empresa sustentavel e estrategica para o pais.
Fanem: seis decadas de inovacao em neonatologia
A Fanem e o caso emblematico de uma empresa brasileira que dominou um nicho global: incubadoras neonatais e equipamentos para cuidado de recem-nascidos. Com mais de 60 anos de operacao, a empresa exporta para mais de 100 paises e demonstra que fabricantes brasileiros de dispositivos medicos podem competir internacionalmente quando investem consistentemente em P&D e qualidade.
O Complexo Economico-Industrial da Saude (CEIS)
O governo federal destinou R$ 57,4 bilhoes ao Complexo Economico-Industrial da Saude (CEIS) no periodo 2024-2026, com o objetivo explicito de reduzir a dependencia externa em produtos de saude. Essa politica publica cria oportunidades concretas para spin-offs biomedicas:
- Parcerias para Desenvolvimento Produtivo (PDPs): acordos entre laboratorios publicos e empresas privadas para internalizar a producao de dispositivos estrategicos
- Margem de preferencia em licitacoes: produtos fabricados no Brasil com tecnologia nacional recebem preferencia de ate 25% em compras publicas
- Encomenda tecnologica (ETEC): o SUS pode contratar diretamente o desenvolvimento de solucoes inovadoras, sem licitacao convencional
- Incentivos fiscais: reducao de IPI e PIS/COFINS para fabricantes nacionais de dispositivos medicos estrategicos
Para pesquisadores e empreendedores, o CEIS sinaliza uma janela de oportunidade historica: o Brasil esta disposto a investir bilhoes para substituir importacoes, e spin-offs que desenvolvam tecnologias alinhadas com as prioridades do complexo encontram um ambiente mais favoravel para financiamento, regulacao e acesso ao mercado.
Em 2024, o governo recebeu 322 propostas de Parcerias para Desenvolvimento Produtivo (147 PDPs e 175 PDILs), com poder de compra potencial de R$ 30 bilhoes por ano pelo SUS.
— Ministerio da Saude / Portaria GM/MS 4.472/2024
Perguntas Frequentes sobre Transferencia Tecnologica em Saude
Quanto tempo leva para ir do laboratorio ao mercado com um dispositivo medico no Brasil?
A media e de 7 a 15 anos, dependendo da classe de risco do dispositivo e da complexidade dos ensaios clinicos necessarios. Dispositivos Classe I (baixo risco) podem chegar ao mercado em 3-5 anos, enquanto dispositivos Classe IV (alto risco) podem demandar 12-15 anos quando se inclui pesquisa basica, desenvolvimento, ensaios clinicos e registro regulatorio.
E possivel manter o vinculo com a universidade ao criar uma spin-off?
Sim. O Marco Legal de CT&I (Lei 13.243/2016) permite que pesquisadores em dedicacao exclusiva participem de atividades em empresas de base tecnologica. E possivel ser socio e ate diretor de uma spin-off, desde que as atividades nao comprometam as obrigacoes academicas. Cada universidade regulamenta os detalhes: a USP, por exemplo, permite ate 8 horas semanais dedicadas a atividades empresariais.
Qual o custo total para registrar um dispositivo medico Classe III na ANVISA?
Para uma empresa de pequeno porte, o custo total regulatorio, incluindo taxa de registro ANVISA (R$ 25.000), certificacao ISO 13485 (R$ 17.000-45.000), testes de conformidade com IEC 60601 (R$ 15.000-40.000) e documentacao tecnica, fica entre R$ 80.000 e R$ 200.000. Esse valor nao inclui ensaios clinicos, que podem adicionar R$ 100.000-500.000 dependendo do numero de pacientes e centros de pesquisa envolvidos.
O que e o modelo tripartite da EMBRAPII e como acessar?
No modelo EMBRAPII, os custos de P&D sao divididos igualmente: 1/3 financiado pela EMBRAPII (recursos nao reembolsaveis), 1/3 pela unidade de pesquisa credenciada e 1/3 pela empresa parceira. Nao ha edital: a empresa procura diretamente uma unidade EMBRAPII credenciada na area de interesse, negocia o escopo do projeto e submete a proposta para aprovacao. O processo costuma levar de 4 a 8 semanas entre o primeiro contato e o inicio do projeto.
Quais certificacoes sao obrigatorias para comercializar um dispositivo medico no Brasil?
As certificacoes minimas sao: registro ou notificacao na ANVISA (conforme a classe de risco), Certificado de Boas Praticas de Fabricacao (CBPF) emitido pela ANVISA, e Autorizacao de Funcionamento de Empresa (AFE). Para dispositivos eletromedicos, e obrigatoria a certificacao de conformidade com a serie IEC 60601 junto ao INMETRO. A ISO 13485 nao e formalmente obrigatoria, mas e pre-requisito pratico para a obtencao do CBPF e para exportacao.
A jornada do laboratorio ao mercado no setor de dispositivos medicos e longa, cara e regulatoriamente complexa, mas o Brasil nunca ofereceu tantos instrumentos de apoio como agora. Com R$ 57,4 bilhoes destinados ao CEIS, um ecossistema crescente de incubadoras hospitalares e programas como EMBRAPII e FAPESP PIPE, pesquisadores e engenheiros biomedicos que compreendem as etapas da translacao tecnologica tem condicoes reais de transformar ciencia em produtos que impactam a saude de milhoes.
Para complementar a compreensao do caminho regulatorio detalhado neste artigo, consulte o guia completo de registro de dispositivos medicos na ANVISA e o artigo sobre financiamento para inovacao em saude. A ANVISA (gov.br/anvisa), a EMBRAPII (embrapii.org.br), o INPI (gov.br/inpi), a FAPESP (fapesp.br/pipe) e o MCTI (gov.br/mcti) sao referencias essenciais para quem inicia a travessia do laboratorio ao mercado.
Artigo produzido pela equipe editorial do Guia Definitivo de Engenharia Biomedica. Atualizado em fevereiro de 2026 com dados do FORMICT/MCTI, ANVISA, EMBRAPII e ABIMO.
Artigos relacionados
Biomateriais: Dos Implantes de Titânio à Bioimpressão 3D [2026]
Guia técnico-científico completo sobre biomateriais na engenharia biomédica: classificação, biocompatibilidade, aplicações clínicas, empresas brasileiras, bioimpressão 3D e mercado global de USD 48 bilhões.
Biomecânica na Engenharia Biomédica [2026]: FEA, Próteses e Análise de Movimento
Guia técnico completo sobre biomecânica na engenharia biomédica: propriedades mecânicas de tecidos, análise de movimento por captura óptica e IA, pipeline de elementos finitos (FEA), design de próteses, implantes ortopédicos, biomecânica cardiovascular e as principais tendências de 2026.
Centros de Pesquisa em Engenharia Biomedica: Mapa Completo do Brasil [2026]
Guia atualizado com mais de 50 centros de pesquisa em engenharia biomedica em 13 estados brasileiros. Conheca os programas com nota CAPES 6 e 7, laboratorios de referencia, linhas de pesquisa, financiamento e como ingressar na pos-graduacao.
Como Publicar Artigos Cientificos em Engenharia Biomedica: Guia Completo [2026]
Guia pratico para publicar artigos cientificos em Engenharia Biomedica: escolha de revistas (Nature BME, IEEE, RBEB), metricas de impacto (JIF, CiteScore, h-index), acesso aberto via CAPES, custos de APC e estrategias para aumentar suas chances de aceite em 2026.