Os dispositivos vestíveis na saúde deixaram de ser gadgets de nicho para se tornar infraestrutura crítica de monitoramento clínico. Em 2024, o mercado global atingiu US\$ 41 bilhões, e as projeções apontam para mais de US\$ 75 bilhões até 2030, impulsionadas por aprovações regulatórias inéditas, miniaturização de hardware e algoritmos de IA que detectam condições cardíacas e metabólicas em tempo real. Para o engenheiro biomédico, esse crescimento representa tanto um campo de atuação em expansão quanto um conjunto de desafios técnicos e regulatórios que precisam ser dominados.
Este artigo faz parte do Guia Definitivo de Engenharia Biomédica.
O Que São Wearables de Saúde e Por Que Importam
Wearables de saúde são dispositivos eletrônicos vestíveis, relógios, patches adesivos, anéis, têxteis inteligentes ou sensores subcutâneos, capazes de coletar, processar e transmitir dados fisiológicos de forma contínua. Diferentemente do equipamento hospitalar tradicional, operam de forma ambulatorial, integrando-se à rotina do paciente sem fios, sem gel condutor e, cada vez mais, sem necessidade de prescrição médica.
A relevância clínica cresceu com a validação científica de sensores não invasivos. Estudos publicados no Journal of the American College of Cardiology demonstraram que algoritmos de ECG em smartwatches detectam fibrilação atrial com 86% de sensibilidade e 94% de especificidade números que justificam o enquadramento como dispositivo médico de Classe II pela ANVISA e pelo FDA. Ao mesmo tempo, o paradigma de edge AI executar inferência de modelos de machine learning diretamente no chip do dispositivo, elimina a dependência de conectividade para alertas críticos e reduz riscos de privacidade.
Para o profissional de engenharia biomédica, dominar esse ecossistema significa transitar entre hardware de ultra-baixo consumo, protocolos de comunicação sem fio, pipelines de TinyML embarcado e frameworks regulatórios nacionais e internacionais. Confira também nossa análise sobre os quatro componentes dos dispositivos médicos vestíveis em ascensão.
Principais Tecnologias de Sensores
Descrição completa da imagem
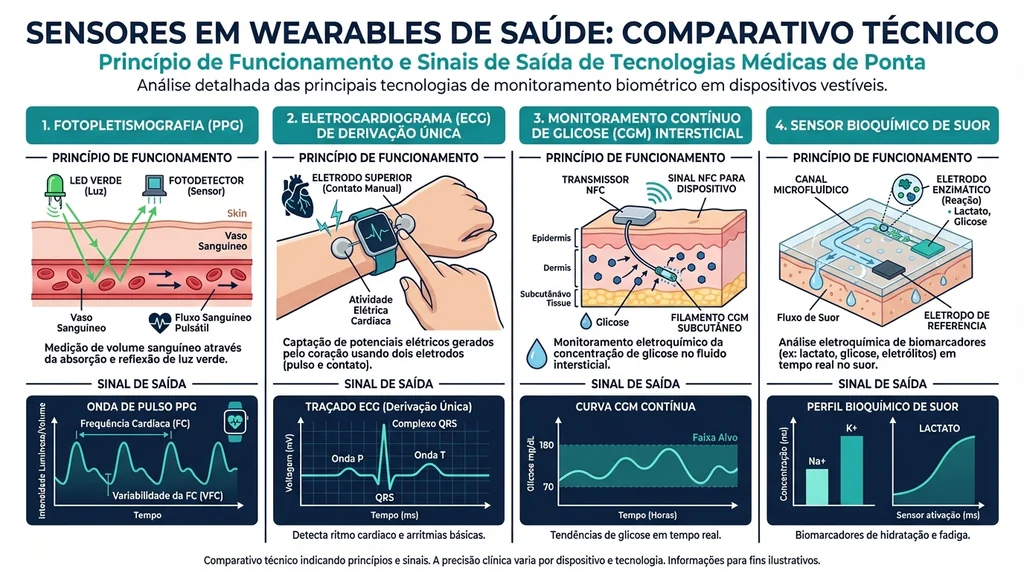
Diagrama técnico comparativo dos quatro principais sensores em wearables de saúde: PPG óptico, ECG de derivação única, CGM intersticial e sensor bioquímico de suor com princípios de funcionamento.
A diversidade de grandezas fisiológicas mensuráveis por wearables cresce a cada ciclo de desenvolvimento. Abaixo, um panorama das principais modalidades em uso clínico e experimental:
Fotopletismografia (PPG)
O sensor PPG emite luz, tipicamente verde a 520 nm para frequência cardíaca e infravermelho para SpO2, e mede a variação de absorção causada pelo fluxo sanguíneo pulsátil. É a base para frequência cardíaca (±2–3 bpm em repouso), saturação de oxigênio (SpO2 ±2%), variabilidade da frequência cardíaca (HRV) e estimativas emergentes de pressão arterial sem manguito. Em julho de 2025, o FDA aprovou os primeiros monitores de pressão arterial baseados em PPG combinado com modelos de aprendizado de máquina para uso em smartwatch, marco regulatório aguardado há anos pela indústria.
Eletrocardiograma Vestível (ECG)
Smartwatches com ECG de derivação única capturam o potencial elétrico cardíaco entre dois pontos: o eletrodo traseiro no pulso e o dedo do usuário encostado na coroa metálica. Patches de longa duração, como o iRhythm Zio XT (14 dias), ampliam a janela de captura, viabilizando detecção de fibrilação atrial paroxística que escaparia de um Holter convencional de 24 horas. O Apple Watch Series 10 e o Samsung Galaxy Watch Ultra foram enquadrados como Classe II pela ANVISA com esse recurso, exigindo notificação, responsável técnico no Brasil e sistema de vigilância pós-mercado.
Monitoramento Contínuo de Glicose (CGM)
O CGM é o wearable médico de maior valor de mercado absoluto entre os segmentos clínicos. Um filamento com enzima glicose-oxidase inserido no interstício subcutâneo gera corrente elétrica proporcional à concentração de glicose, transmitida a cada 1–5 minutos via BLE ou NFC. O mercado global de CGM alcançou US\$ 10,9–13,7 bilhões em 2024, com Abbott (56,3% de participação, FreeStyle Libre 3 com MARD de 7,9%) e Dexcom (35,2%) dominando. Em 2024, o FDA aprovou o primeiro CGM sem prescrição para adultos não diabéticos, expandindo radicalmente o mercado de bem-estar metabólico.
O mercado de CGMs concentra 98,8% de participação em apenas três fabricantes: Abbott (56,3%), Dexcom (35,2%) e Medtronic (6,9%). O Dexcom Stelo, aprovado pela FDA em março de 2024, tornou-se o primeiro CGM vendido sem prescrição nos EUA.
— FDA / Relatórios de mercado CGM, 2024
| Sensor | Grandeza Mensurada | Precisão Típica | Maturidade de Mercado |
|---|---|---|---|
| PPG | FC, SpO2, HRV | ±2 bpm / ±2% SpO2 | Comercial consolidado |
| ECG 1 derivação | Ritmo cardíaco, FA | Sens. 86% / Espec. 94% | Classe II (FDA/ANVISA) |
| CGM (intersticial) | Glicose | MARD 7,9–9,2% | Comercial, prescrito/OTC |
| Acelerômetro / IMU | Movimento, queda, sono | Varia por algoritmo | Comercial consolidado |
| Sensor de suor bioquímico | Cortisol, lactato, Na+ | Em validação clínica | Pesquisa / protótipos |
| E-tattoo / eletrônica flexível | EMG, EEG, ECG flexível | Em validação clínica | Pesquisa avançada |
Hardware: Chips, Protocolos e Arquitetura de Sistemas

O projeto de hardware para wearables médicos exige equilíbrio entre poder computacional, consumo energético e tamanho físico. Os microcontroladores e SoCs mais adotados em 2025–2026 são:
- Nordic nRF5340 dual-core ARM Cortex-M33 com rádio BLE 5.3/Thread nativo; consumo em modo conectado abaixo de 5 mA. É a referência para hubs BLE de baixo consumo em patches e smartwatches de segmento médico.
- STM32U5 (ST Microelectronics), certificado PSA Nível 3, consumo em run mode de 19 µA/MHz, suporte a TrustZone para armazenamento seguro de chaves criptográficas. Presente em mais de 20 milhões de dispositivos IoT médicos ativos.
- MAX78000 (Analog Devices), combina microcontrolador ARM com acelerador CNN de ultra-baixo consumo, realizando inferência abaixo de 1 mW. Ideal para análise de ECG embarcada e detecção de arritmias sem envio de dados brutos à nuvem.
A comunicação sem fio segue protocolos distintos conforme o caso de uso: BLE 5.x para conexão com smartphone (range até 400 m, taxa até 2 Mbps, suficiente para ECG e PPG comprimido), NFC para leitura passiva de patches (FreeStyle Libre 2 usa ISO 15693, sem bateria ativa no sensor durante a leitura) e LoRaWAN para telemetria de longa distância, alcance de 10–15 km em área aberta, estudado para monitoramento rural no Brasil em municípios sem cobertura celular adequada.
O paradigma de edge AI ganhou tração porque reduz latência de alertas (abaixo de 200 ms), consumo de banda e riscos de privacidade. Modelos de redes neurais treinados em PyTorch são quantizados para int8/int4 e convertidos para rodar diretamente no microcontrolador, detectando FA, hipoglicemia ou queda localmente, transmitindo apenas alertas e metadados comprimidos para a nuvem.
Meta-análise de 2025 publicada no JACC: Advances demonstrou que a detecção de fibrilação atrial por smartwatches alcança 86% de sensibilidade e 94% de especificidade, consolidando wearables como ferramentas de rastreamento cardiovascular clinicamente relevantes.
— JACC: Advances, Meta-análise de Detecção de FA por Smartwatches, 2025
Regulamentação no Brasil: ANVISA e RDCs Chave
No Brasil, wearables com claims clínicos são classificados como Produtos para Saúde e exigem registro ou notificação na ANVISA antes da comercialização. As normativas fundamentais são:
- RDC 751/2022 regulamento técnico geral para dispositivos médicos, alinhado ao framework IMDRF e estruturalmente equivalente ao Regulation (EU) 2017/745 europeu. Estabelece classificação por risco (Classe I a IV) e exigências de evidência clínica.
- RDC 657/2022 dedicada a Software como Dispositivo Médico (SaMD), abrangendo algoritmos de detecção de FA, apneia e pressão arterial em smartwatches. Classifica o software por severidade do impacto clínico (I a IV) conforme IMDRF.
| Aspecto | Exigência ANVISA |
|---|---|
| Classificação de risco | Classe I a IV; ECG vestível = Classe II |
| Tipo de registro | Notificação (Classe II) ou Registro completo (Classe III/IV) |
| SaMD | RDC 657/2022, validação de software e rastreabilidade de versões |
| Importação | Certificado de Boas Práticas de Fabricação (BPF) do país de origem |
| Vigilância pós-mercado | Responsável técnico no Brasil, sistema de notificação de eventos adversos |
O Apple Watch com função ECG e o Samsung Galaxy Watch Ultra com detecção de FA foram enquadrados como Classe II pela ANVISA. Um smartwatch idêntico comercializado apenas com claims de bem-estar (passos, calorias) pode ser isento de registro, o enquadramento depende inteiramente da destinação declarada pelo fabricante. Para mais detalhes sobre o processo regulatório, consulte nosso artigo sobre regulamentação ANVISA de dispositivos médicos e o portal oficial da ANVISA.
Regulamentação Internacional: FDA e Marcos Recentes
O FDA opera como referência global para validação clínica de wearables. As aprovações recentes com maior impacto no mercado mundial e no pipeline regulatório brasileiro:
| Marco Regulatório | Data | Impacto |
|---|---|---|
| CGM sem prescrição (OTC) | 2024 | Abbott Lingo e Dexcom Stelo disponíveis sem receita para adultos não diabéticos |
| Detecção de apneia em smartwatch | 2024 | Apple Watch aprovado para triagem de apneia do sono por acelerometria |
| Monitor de PA sem manguito | Jul/2025 | Primeira aprovação para mensuração contínua via PPG + ML em smartwatch de consumo |
| De Novo ECG vestível (múltiplos) | 2018–2024 | Apple Watch, Withings ScanWatch, Fitbit Sense 2, precedente consolidado |
Essas aprovações criam precedente para que a ANVISA siga trajetória similar, reduzindo o gap regulatório que historicamente atrasava o acesso de brasileiros a tecnologias aprovadas no exterior. O banco de dados de aprovações do FDA (510(k) Database) está disponível em fda.gov/medical-devices e é referência obrigatória para benchmarking técnico e estratégia regulatória.
LGPD e Privacidade de Dados de Saúde
Descrição completa da imagem
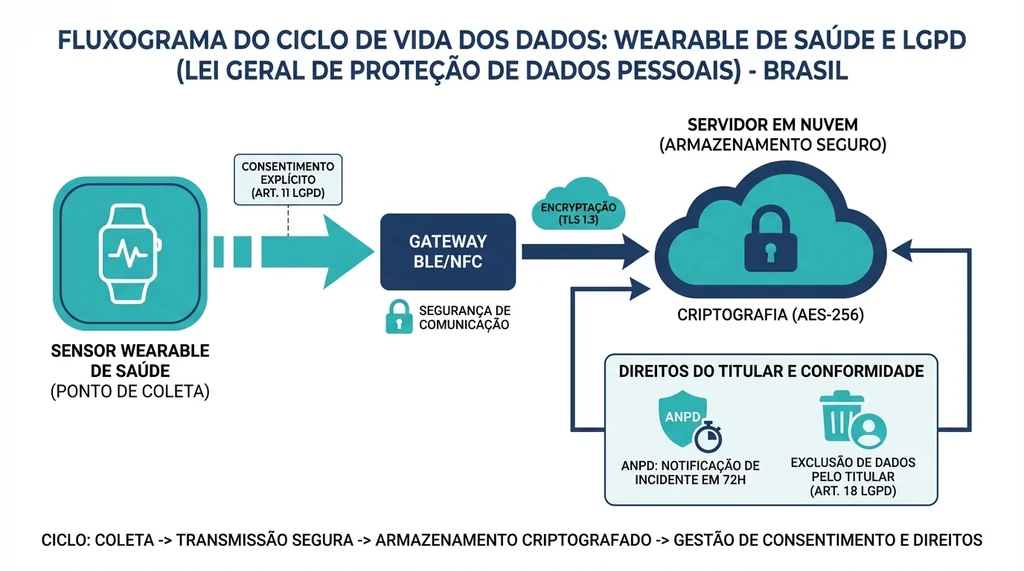
Fluxograma do ciclo de vida de dados de wearables de saúde conforme a LGPD brasileira, coleta, transmissão criptografada, armazenamento seguro, consentimento explícito e direitos do titular.
Dados coletados por wearables de saúde se enquadram como dados pessoais sensíveis nos termos da Lei Geral de Proteção de Dados (LGPD, Lei 13.709/2018), exigindo consentimento explícito e específico para coleta e tratamento. Implicações práticas para o desenvolvedor e fabricante:
- Armazenamento local no dispositivo ou em nuvem com criptografia AES-256 em repouso e TLS 1.3 em trânsito.
- Controle de acesso granular: o usuário deve poder exportar, corrigir e solicitar exclusão de seus dados (direitos do titular, Art. 18 LGPD).
- Relatório de Impacto à Proteção de Dados Pessoais (RIPD) recomendado pela ANPD para aplicações de monitoramento de saúde.
- Transmissão de dados para servidores fora do Brasil exige verificação de adequação do país receptor ou adoção de cláusulas contratuais padrão reconhecidas pela ANPD.
- Notificação de incidentes de segurança à ANPD em até 72 horas após ciência, com comunicação ao titular afetado.
Caso Brasileiro de Destaque: brain4care
A startup brasileira brain4care desenvolveu um sensor não invasivo para monitoramento contínuo da pressão intracraniana (PIC), grandeza que, até então, exigia procedimentos cirúrgicos invasivos com craniotomia. O dispositivo analisa a morfologia do pulso arterial periférico para inferir variações da PIC, sem qualquer penetração craniana. Obteve autorização do FDA em 2021 e hoje está presente em mais de 80 hospitais em diferentes países.
A brain4care, fundada em 2014 pelo físico Sérgio Mascarenhas, acumula mais de 83 publicações científicas e foi reconhecida como Technology Pioneer 2025 pelo Fórum Econômico Mundial e Deep Tech of the Year 2024, projetando receita global de US$ 1 bilhão até 2030.
— World Economic Forum / brain4care, 2025
O caso ilustra o caminho viável para deep techs brasileiras: foco em problema clínico não resolvido, validação técnica robusta em centros de pesquisa, busca simultânea de registro nacional (ANVISA) e internacional (FDA/CE) e escalabilidade global desde o início. A empresa é frequentemente citada em publicações do IEEE Engineering in Medicine and Biology Society (EMBS) como exemplo de inovação de alto impacto originada no Brasil.
Fronteiras da Tecnologia: Sensores de Suor, E-Tattoos e Smart Textiles
Três frentes de inovação concentram a atenção da pesquisa acadêmica e dos grandes players industriais para o período 2026–2030:
Sensores Bioquímicos de Suor
Patches microfluídicos com eletrodos enzimáticos permitem medir cortisol (marcador de estresse fisiológico e resposta ao exercício), lactato (performance esportiva e triagem de sepse precoce) e eletrólitos como Na+ e K+ diretamente no suor, em tempo real e sem punção. Grupos do MIT, UC Berkeley e Universidade de São Paulo publicaram resultados promissores, mas a variabilidade da composição do suor entre indivíduos e ao longo do tempo ainda é o principal desafio de calibração, problema que deve ser resolvido nos próximos 2–3 anos.
E-Tattoos e Eletrônica Flexível
Eletrodos ultrafinos impressos em substratos poliméricos conformam-se à pele como uma tatuagem temporária, captando sinais de EMG, EEG e ECG com qualidade comparável a eletrodos clínicos rígidos. Startups como Delsys e grupos de pesquisa da UT Austin lideram publicações no IEEE Transactions on Biomedical Engineering (TBME). A vantagem é a conformidade mecânica perfeita com o corpo, reduzindo artefatos de movimento que afetam eletrodos convencionais.
Smart Textiles
Tecidos com fios condutores integrados permitem monitorar frequência cardíaca, frequência respiratória e temperatura corporal sem nenhum dispositivo adicional além da roupa. O desafio de lavabilidade, manter condutividade elétrica após múltiplos ciclos de lavagem, e durabilidade mecânica dos eletrodos têxteis é o principal gargalo para adoção clínica em larga escala.
Para um panorama mais amplo das tendências que estão remodelando a engenharia biomédica, veja nosso artigo sobre tendências e futuro da engenharia biomédica.
Oportunidades para Engenheiros Biomédicos no Ecossistema de Wearables
O crescimento do setor cria demanda em ao menos quatro perfis profissionais distintos, cada um com competências específicas:
| Perfil Profissional | Competências-chave | Onde Atuar |
|---|---|---|
| Engenheiro de Hardware | Circuitos analógicos de aquisição, layout PCB flexível, consumo ultra-baixo, BLE | Startups, fabricantes OEM, institutos de P&D |
| Engenheiro de Firmware | RTOS, BLE stack, processamento de sinal embarcado, TinyML | Startups, empresas de saúde digital |
| Cientista de Dados Clínicos | ML para séries temporais fisiológicas, validação clínica, estatística biomédica | Hospitais, healthtechs, centros de pesquisa |
| Especialista Regulatório | ANVISA RDC 751/657, FDA 510(k)/De Novo, ISO 13485, IEC 62304 | Consultorias, indústria de dispositivos médicos |
O mercado cresce mais rápido do que a oferta de profissionais qualificados. A combinação de domínio técnico (hardware + firmware + ML embarcado) com conhecimento regulatório (ANVISA + FDA + LGPD) é especialmente valorizada, e rara no mercado brasileiro atual.
FAQ: Perguntas Frequentes sobre Wearables na Saúde
Todo smartwatch com sensor de frequência cardíaca precisa de registro na ANVISA?
Não necessariamente. O enquadramento depende do claim comercial. Dispositivos posicionados apenas como trackers de bem-estar (passos, calorias) geralmente são isentos. Se há indicação de monitoramento de condição clínica (FA, arritmia, hipóxia), o registro de Classe II é obrigatório. A ANVISA avalia caso a caso com base na destinação declarada pelo fabricante, e o software de interpretação (SaMD) também entra nessa análise conforme a RDC 657/2022.
Qual a diferença prática entre CGM e monitor de glicemia capilar?
O CGM mede glicose intersticial de forma contínua (a cada 1–5 minutos) via sensor subcutâneo, sem picadas frequentes, e entrega tendências e alertas preditivos de hipo/hiperglicemia antes que o paciente sinta sintomas. O monitor capilar faz leituras pontuais com amostra de sangue, mais preciso por medir diretamente no sangue, mas sem continuidade. O CGM é superior para ajuste de insulina em tempo real e gestão de DM1/DM2 instável; o capilar ainda é padrão para confirmação diagnóstica e calibração em alguns sistemas.
Como o edge AI se aplica a wearables médicos na prática?
Modelos de redes neurais compactos são quantizados e executados no microcontrolador do próprio dispositivo. Um exemplo concreto: o MAX78000 pode rodar um classificador de arritmias treinado em PyTorch, convertido via MAX78000 Model Converter para operação com acelerador CNN interno, consumindo menos de 1 mW durante a inferência. Isso permite alertar o usuário sobre eventos cardíacos em menos de 200 ms, sem depender de conectividade com smartphone ou nuvem, crítico em situações de emergência.
Dados de wearables podem ser usados como evidência em prontuário eletrônico?
Depende do enquadramento regulatório e da validação clínica do dispositivo. Dados de dispositivos Classe II com estudos de acurácia publicados têm maior aceitação em contextos clínicos. A tendência é de integração progressiva via HL7 FHIR com sistemas de saúde hospitalares, padrão de interoperabilidade já adotado por Apple Health, Google Health e principais HIS brasileiros. O CFM ainda não emitiu resolução específica sobre prontuário eletrônico com dados de wearables, mas o tema está na agenda regulatória.
O que é necessário para desenvolver um wearable médico no Brasil do zero?
O desenvolvimento exige ao menos quatro etapas paralelas: (1) projeto técnico hardware, firmware, algoritmos e testes de bancada; (2) validação clínica estudo com pacientes para demonstrar acurácia e segurança; (3) conformidade regulatória dossiê para ANVISA (RDC 751/2022 + RDC 657/2022 para SaMD) e eventual FDA/CE para exportação; (4) conformidade com LGPD arquitetura de privacidade desde o design. Financiamento via FINEP, FAPESP ou BNDES Inovação pode apoiar a fase de P&D de alto risco.
Wearables de saúde representam uma das intersecções mais dinâmicas entre eletrônica, ciência de dados, regulamentação e medicina clínica. O engenheiro biomédico que dominar esse ecossistema, da escolha do sensor ao processo regulatório, passando pelo firmware e pela conformidade com LGPD, estará posicionado em um mercado que crescerá quase 90% na segunda metade desta década.
Para aprofundar sua formação e explorar as demais áreas da engenharia biomédica, acesse o Guia Definitivo de Engenharia Biomédica.
Artigo elaborado pela equipe editorial com base em dados de mercado, publicações do IEEE EMBS documentação regulatória da ANVISA e do FDA e estudos clínicos peer-reviewed. Última atualização: fevereiro de 2026.
Artigos relacionados
Cirurgia Robótica no Brasil: 417% de Crescimento e o Papel do Engenheiro Biomédico
De 2 robôs em 2008 a 200 plataformas em 2025, o Brasil realizou 120 mil procedimentos robóticos acumulados e se tornou o 9º mercado mundial. Entenda o ecossistema de plataformas, regulamentação ANVISA/CFM, financiamento ANS e como o engenheiro biomédico é peça central nessa revolução.
Healthtechs Brasileiras: Mapa Completo do Ecossistema com 1.900+ Startups [2026]
O ecossistema de healthtechs Brasil reúne 1.900+ startups, movimenta US$ 6,34 bilhões e concentra 64,8% do investimento em saúde digital da América Latina.
Inteligência Artificial na Saúde Brasileira: O Mapa Completo para Engenheiros Biomédicos [2026]
Panorama completo da inteligência artificial na saúde brasileira em 2026: dados, regulação, mercado e oportunidades para engenheiros biomédicos.
Informática em Saúde: HIS, Prontuário Eletrônico e Interoperabilidade FHIR/HL7 [2026]
Guia completo sobre informática em saúde: HIS, prontuário eletrônico do paciente, padrões HL7 e FHIR, interoperabilidade, RNDS, mercado brasileiro e carreira para engenheiros biomédicos.