Três aprovações do FDA em um único ciclo de inovação: em 2025, a GE HealthCare recebeu autorização regulatória para o AIR Recon DL aplicado à cardiologia, para os gradientes supercondutores MAGNUS e para a integração do software NeuroQuant à plataforma SIGNA de ressonância magnética. O conjunto de aprovações representa o maior avanço tecnológico da linha SIGNA desde a introdução do campo de 3 Tesla no ambiente clínico, e reposiciona a GE HealthCare na disputa com Siemens Healthineers e Philips Healthcare em um mercado global de equipamentos de RM avaliado em US$ 8,4 bilhões em 2024.
Este artigo faz parte do Guia Definitivo de Engenharia Biomédica.
A Plataforma SIGNA: Histórico e Posicionamento no Mercado Global de RM
A plataforma SIGNA existe desde 1982, quando a GE Medical Systems instalou o primeiro sistema SIGNA 1.5T em um hospital universitário dos Estados Unidos. Ao longo de quatro décadas, a linha evoluiu de magnetos resistivos para supercondutores, incorporou bobinas de radiofrequência (RF) de múltiplos canais, sequências de pulso aceleradas e, mais recentemente, algoritmos de reconstrução baseados em deep learning. Hoje, a família SIGNA inclui modelos de 1.5T (SIGNA Artist, SIGNA Voyager), 3T (SIGNA Premier, SIGNA Architect) e 7T (SIGNA Magnus, voltado à pesquisa), além do SIGNA Architect de gradiente ultra-alto desenhado para neurorradiologia de alta resolução.
No mercado global, a GE HealthCare mantém participação de aproximadamente 28% no segmento de ressonância magnética posicionando-se como a segunda maior fabricante do mundo, atrás da Siemens Healthineers (33%) e à frente da Philips Healthcare (22%), segundo relatório da GlobalData publicado em 2025. No Brasil, a GE HealthCare é fornecedora de sistemas SIGNA para redes hospitalares de grande porte como o Hospital Albert Einstein, o Hospital Sírio-Libanês e unidades da Rede D'Or São Luiz, além de hospitais universitários vinculados ao MEC.
A plataforma SIGNA é relevante para além de seu volume de vendas: ela serve como base tecnológica sobre a qual os três recursos recém-aprovados pelo FDA foram desenvolvidos. Compreender a arquitetura da plataforma, magneto supercondutor, bobinas de RF, sistema de gradientes, cadeias de aquisição e software de reconstrução, é essencial para avaliar o impacto clínico de cada aprovação. Para profissionais que atuam em engenharia clínica e P&D de equipamentos médicos as especificações técnicas dessas aprovações definem os parâmetros de performance que balizam a próxima geração de protocolos de RM.
Primeira Aprovação: AIR Recon DL para Cardiorressonância
O AIR Recon DL (Deep Learning) já existia na plataforma SIGNA para aplicações neurológicas e musculoesqueléticas desde 2020, quando recebeu sua primeira autorização de comercialização do FDA. A aprovação de 2025 estende o algoritmo de forma específica para cardiorressonância magnética (cardiac MRI) uma indicação tecnicamente distinta e muito mais exigente do ponto de vista de reconstrução de imagem.
O desafio central da RM cardíaca é a natureza cíclica e não-estacionária do objeto de interesse: o coração bate em média 60 a 100 vezes por minuto, e qualquer aquisição que não sincronize com o ciclo cardíaco produz artefatos de movimento que tornam a imagem clinicamente inutilizável. Os protocolos convencionais usam gatilhamento eletrocardiográfico (ECG-gating) para adquirir dados apenas em fases específicas do ciclo, prolongando o tempo de exame para 45 a 90 minutos em pacientes cooperativos, e tornando o exame inviável em pacientes com arritmias ou que não conseguem prender a respiração por períodos prolongados.
O AIR Recon DL cardíaco opera em duas etapas distintas. Na primeira, uma rede neural convolucional profunda, treinada sobre mais de 400.000 pares de imagens cardíacas adquiridas em múltiplos campos magnéticos e protocolos aplica supressão de ruído adaptativa no domínio do espaço-k antes da reconstrução de Fourier. Na segunda, o algoritmo identifica e compensa retroativamente artefatos residuais de movimento cardíaco. O resultado clínico documentado nos estudos enviados ao FDA é uma redução de 40 a 60% no tempo de aquisição de exames padrão de cardio RM (cine SSFP, mapeamento de T1/T2 miocárdico, realce tardio com gadolínio) sem degradação perceptível da qualidade de imagem avaliada por radiologistas especialistas.
Para hospitais que operam aparelhos SIGNA 1.5T e 3T instalados, o AIR Recon DL cardíaco é disponibilizado como atualização de software, sem necessidade de substituição do hardware físico. Essa característica é relevante no contexto brasileiro, onde o ciclo de renovação de equipamentos de RM em hospitais públicos pode superar 15 anos.

Segunda Aprovação: Sistema de Gradientes MAGNUS
Os gradientes de campo magnético são o componente do sistema de RM responsável pela codificação espacial do sinal. Sua performance é definida por dois parâmetros críticos: a amplitude máxima (em mT/m, que determina a resolução espacial alcançável) e o slew rate (em T/m/s, que define a velocidade com que o gradiente pode ser ativado e desativado, determinando a resolução temporal e a velocidade de aquisição). Em sistemas convencionais de 3T, a amplitude máxima típica é de 40 a 45 mT/m com slew rate de 200 T/m/s.
O sistema MAGNUS, sigla para MAgnitude GradieNt Upgrade System, representa uma ruptura com essa arquitetura padrão. O conjunto de gradientes supercondutores desenvolvido pela GE HealthCare atinge 200 mT/m de amplitude com slew rate de 500 T/m/s números que até então eram exclusivos de sistemas de pesquisa de ultra-alto campo (7T) ou de protótipos experimentais como o Connectom (3T, 300 mT/m, 200 T/m/s) desenvolvido pelo Human Connectome Project em parceria com a Siemens e o NIH.
| Parâmetro | SIGNA Convencional 3T | SIGNA MAGNUS | Conectom (Pesquisa) |
|---|---|---|---|
| Amplitude máxima de gradiente | 45 mT/m | 200 mT/m | 300 mT/m |
| Slew rate máximo | 200 T/m/s | 500 T/m/s | 200 T/m/s |
| Campo magnético | 3T | 3T | 3T |
| Indicação primária | Diagnóstico geral | Neuroimagem / Difusão | Pesquisa de conectividade |
| Aprovação FDA | Sim | Sim (2025) | Uso em pesquisa |
As implicações clínicas de gradientes de maior amplitude são profundas especialmente para imagens ponderadas em difusão (DWI) e tractografia de fibras brancas (DTI). Com o MAGNUS, é possível atingir valores de b superiores a 5.000 s/mm² sem o aumento proporcional de tempo de aquisição observado em gradientes convencionais. Isso permite a resolução de microestruturas neuronais, como axônios de pequeno diâmetro e estruturas da substância branca profunda, que eram anteriormente invisíveis em RM clínica de 3T. A aplicação imediata mais relevante é na diferenciação entre tumores primários do SNC e metástases, além do mapeamento pré-cirúrgico de tratos do sistema nervoso em neurocirurgia.
O MAGNUS também impacta a RM de corpo inteiro com difusão (whole-body DWI) utilizada no estadiamento oncológico. Ao reduzir o tempo total de aquisição em até 50%, o protocolo torna-se viável para pacientes com limitações de cooperação, idosos, pacientes oncológicos em tratamento quimioterápico ativo, ou portadores de condições que limitam a capacidade de permanecer imóvel por longos períodos.
Terceira Aprovação: Integração do NeuroQuant à Plataforma SIGNA
A terceira aprovação envolve a integração nativa do NeuroQuant software de volumetria cerebral automatizada desenvolvido pela CorTechs Labs, diretamente ao workflow da plataforma SIGNA, sem necessidade de exportação manual de imagens para servidores externos. O NeuroQuant recebeu sua primeira autorização do FDA em 2006 para quantificação do volume do hipocampo em pacientes com suspeita de Doença de Alzheimer, sendo pioneiro no uso clínico de segmentação automatizada de estruturas cerebrais por RM.
Na versão integrada ao SIGNA, o processo funciona da seguinte forma: ao término de uma sequência de RM 3D T1 isotrópica (como a MPRAGE, Magnetization Prepared Rapid Gradient Echo, com resolução de 1 mm³), o sistema automaticamente envia os dados ao módulo NeuroQuant, que segmenta 45 estruturas cerebrais subcorticais em menos de 10 minutos. O relatório gerado compara os volumes de cada estrutura com um banco de dados normativo estratificado por idade, sexo e campo magnético, apresentando percentis de normalidade ao radiologista.
As indicações clínicas aprovadas incluem demências neurodegenerativas (Alzheimer, demência frontotemporal, demência de corpos de Lewy), epilepsia (avaliação de esclerose hipocampal), esclerose múltipla (quantificação de atrofia cortical e de substância cinzenta profunda) e traumatismo cranioencefálico (TBI). Em estudos de validação apresentados ao FDA, o NeuroQuant demonstrou variabilidade de medição intra e interobservador inferior a 2%, contra 8 a 15% para medições manuais por radiologistas experientes.
Para o contexto brasileiro, a integração nativa do NeuroQuant ao SIGNA é especialmente relevante considerando que o Brasil possui 2,7 milhões de pessoas com demência segundo dados da Alzheimer's Disease International (2023), número que deverá triplicar até 2050 com o envelhecimento da população. A volumetria hipocampal automatizada por RM é um biomarcador de imagem reconhecido pelos critérios diagnósticos NIA-AA (National Institute on Aging–Alzheimer Association) de 2018 para diagnóstico de Doença de Alzheimer em fase pré-clínica e demencial.
Deep Learning na Reconstrução de Imagens de RM: O Que Mudou
Para compreender o impacto do AIR Recon DL, e por que ele representa uma mudança de paradigma real, não apenas incremental, é necessário entender o processo tradicional de reconstrução de imagens em RM.
Em um sistema convencional, o sinal de RF emitido pelos prótons do tecido é capturado pelas bobinas receptoras, digitalizado e armazenado no espaço-k (domínio da frequência espacial). A imagem final é obtida pela transformada de Fourier inversa desse espaço-k. O ruído presente na imagem é intrínseco ao processo de aquisição e proporcional à raiz quadrada do número de médias adquiridas (NEX ou NSA). Para reduzir o ruído pela metade, é necessário quadruplicar o número de médias, e, portanto, quadruplicar o tempo de exame.
O AIR Recon DL contorna essa limitação fundamental ao aplicar uma rede neural U-Net modificada para distinguir sinal real de ruído estocástico no espaço-k e no domínio da imagem simultaneamente. A rede foi treinada com técnica de aprendizado supervisionado: imagens com baixa SNR (poucas médias, tempo curto) foram emparelhadas com imagens de alta SNR (muitas médias, tempo longo) adquiridas do mesmo plano e estrutura anatômica. O modelo aprendeu a mapear diretamente de imagens ruidosas para imagens de alta qualidade, generalizando para anatomias, patologias e campos magnéticos não vistos no treinamento.
O resultado prático documentado em publicações peer-reviewed, incluindo estudos publicados no Journal of Magnetic Resonance Imaging e no Radiology é consistente: redução de ruído de 40 a 70% com preservação ou melhora de nitidez de bordas especialmente em estruturas de tecido mole com baixo contraste natural (cartilagem, nervo periférico, plexo braquial). O ganho em SNR equivalente permite ou reduzir o tempo de aquisição em proporção similar ou aumentar a resolução espacial sem penalidade temporal.
É importante ressaltar que o AIR Recon DL não é o único algoritmo de reconstrução por deep learning aprovado pelo FDA no segmento de RM. A Siemens Healthineers possui o Deep Resolve, a Philips o SmartSpeed e a Canon o Advanced intelligent Clear-IQ Engine (AiCE). A diferença competitiva entre eles está nas arquiteturas de rede, nos conjuntos de dados de treinamento e, criticamente, no desempenho em anatomias específicas e patologias específicas, como o caso cardíaco da aprovação mais recente da GE HealthCare.
Contexto Regulatório: Como o FDA Aprova Software de IA para Dispositivos Médicos
As três aprovações da GE HealthCare passaram por vias regulatórias distintas no FDA, o que ilustra a complexidade crescente da regulamentação de software baseado em inteligência artificial para dispositivos médicos, um tema diretamente relevante para profissionais que atuam em regulamentação de dispositivos médicos.
O AIR Recon DL cardíaco e o NeuroQuant integrado foram autorizados via 510(k) clearance que exige demonstração de equivalência substancial a um predicate device previamente autorizado. No caso do AIR Recon DL, o predicate foi a versão original do algoritmo aprovada em 2020 para neuroimagem. Para o NeuroQuant, o predicate foi o software standalone aprovado em 2006. Em ambos os casos, a GE HealthCare precisou demonstrar que as novas funcionalidades não introduziam novos riscos em relação aos predicates, um processo que inclui estudos clínicos de validação de desempenho do algoritmo (algorithm performance studies) com conjuntos de dados prospectivos.
O sistema MAGNUS de gradientes seguiu caminho diferente: como representa um avanço de hardware sem predicate direto comparável em desempenho, foi submetido ao processo De Novo que cria uma nova classe de dispositivo e estabelece os critérios de performance para futuros competidores. O De Novo exige que o fabricante defina os Special Controls, requisitos técnicos específicos de performance e segurança, que passarão a valer como referência para o mercado.
No Brasil, a trajetória regulatória para dispositivos equivalentes é distinta. A ANVISA classifica e registra equipamentos de RM sob a égide da RDC nº 751/2022 (regulamentação de dispositivos médicos), enquanto softwares de auxílio diagnóstico como o AIR Recon DL e o NeuroQuant seguem a RDC nº 657/2022, específica para Software como Dispositivo Médico (SaMD). A aceitação de dados clínicos gerados no exterior para registro nacional, a chamada equivalência regulatória, é possível, mas condicionada ao cumprimento de requisitos adicionais de pós-mercado definidos caso a caso pela ANVISA.
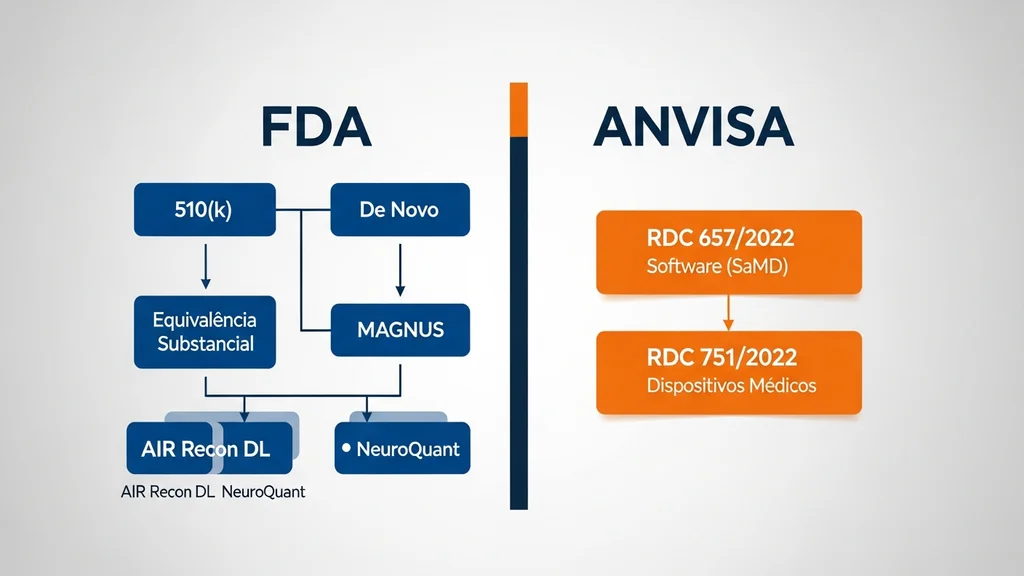
Descrição completa da imagem
Fluxograma comparativo do processo de aprovação FDA 510k e De Novo versus ANVISA RDC 657 para software de IA em ressonância magnética.
Impacto no Mercado Brasileiro de Ressonância Magnética
O Brasil possui aproximadamente 3.200 equipamentos de ressonância magnética instalados segundo o Cadastro Nacional de Estabelecimentos de Saúde (CNES) de 2025, com distribuição fortemente concentrada nas regiões Sudeste (58%) e Sul (17%). A densidade de RM por habitante, cerca de 15 aparelhos por milhão de habitantes, é significativamente inferior à média da OCDE (aproximadamente 60 por milhão), o que revela tanto a dimensão do subacesso quanto o potencial de crescimento do mercado.
A base instalada de equipamentos SIGNA no Brasil é estimada em torno de 700 a 900 unidades em operação, com modelos que variam desde SIGNA 1.5T com mais de 10 anos de uso em hospitais públicos até instalações recentes de SIGNA Premier 3T em centros privados de diagnóstico por imagem. As aprovações de 2025 têm impacto distinto dependendo do segmento:
Para o setor privado de diagnóstico por imagem as aprovações criam diferencial competitivo imediato: clínicas que operam SIGNA Premier 3T podem oferecer protocolos de cardio RM com tempo reduzido (exames que duravam 75 minutos podem ser realizados em 35 a 45 minutos), aumentando o giro de exames e reduzindo custos por procedimento. O NeuroQuant integrado adiciona laudos quantitativos de volumetria cerebral sem custo marginal de software adicional, um diferencial para centros de neurologia e memória.
Para os hospitais universitários e centros de pesquisa o sistema MAGNUS abre possibilidades de estudos de microestrutura cerebral que anteriormente exigiam acesso a equipamentos de pesquisa de 7T ou ao Connectom, disponível em número muito limitado no mundo. Universidades brasileiras com programas de pós-graduação em neurociências, como a USP, UNICAMP e UFMG, estão entre os potenciais beneficiários diretos da aprovação do MAGNUS para uso clínico-acadêmico.
Para o SUS o impacto mais imediato das aprovações é indireto: a redução no tempo de exame propiciada pelo AIR Recon DL pode aumentar a produtividade dos aparelhos instalados em hospitais federais e estaduais sem necessidade de investimento em novo hardware. Um equipamento que realiza 8 exames de RM por turno de 8 horas pode chegar a 12 a 14 com protocolos acelerados por deep learning, um ganho de throughput relevante em contexto de lista de espera significativa. Para uma análise mais ampla do setor de dispositivos médicos no Brasil, veja o artigo sobre o mercado de dispositivos médicos no Brasil.
Perspectivas para Engenheiros Biomédicos: Oportunidades e Competências
As três aprovações da GE HealthCare criam demandas técnicas específicas que moldam o perfil de competências procurado pelo mercado. Para profissionais que atuam ou pretendem atuar no segmento de equipamentos de diagnóstico por imagem, as oportunidades se organizam em quatro frentes:
Aplicações clínicas e suporte técnico especializado: A implementação de protocolos de AIR Recon DL cardíaco e NeuroQuant em hospitais exige profissionais capazes de configurar workflows integrados no sistema de informação radiológica (RIS/PACS), calibrar parâmetros de aquisição para maximizar o desempenho dos algoritmos de DL, e treinar equipes técnicas de RM. Esse perfil, denominado Clinical Application Specialist ou CAS, é recrutado ativamente por GE HealthCare, Siemens Healthineers e Philips em todo o Brasil.
Engenharia de manutenção e qualidade de equipamentos: O sistema de gradientes MAGNUS opera com correntes muito superiores às de sistemas convencionais, o que impõe novos requisitos de manutenção preventiva, monitoramento de temperatura do cryostat e gerenciamento de quench. Engenheiros clínicos que dominam a física dos supercondutores e os protocolos de manutenção de gradientes de alta performance têm posicionamento diferenciado. Para uma visão das diferentes áreas de atuação em engenharia biomédica, consulte o artigo sobre áreas de atuação da engenharia biomédica.
Regulamentação e acesso ao mercado: A complexidade crescente dos processos 510(k), De Novo no FDA e RDC 657/2022 na ANVISA para softwares de IA em dispositivos médicos cria demanda crescente por engenheiros regulatórios especializados em SaMD (Software as a Medical Device). Profissionais com formação em engenharia biomédica e especialização em assuntos regulatórios estão entre os perfis com maior escassez relativa no Brasil, segundo dados da Abimo.
Pesquisa e desenvolvimento de algoritmos: As redes neurais aplicadas à reconstrução de RM, à segmentação de estruturas cerebrais e à compensação de movimento cardíaco são campos ativos de pesquisa acadêmica e industrial. No Brasil, grupos de pesquisa na USP (Instituto de Física de São Carlos), UNICAMP (Faculdade de Engenharia Elétrica) e UERJ desenvolvem algoritmos de processamento de imagens médicas com potencial de aplicação clínica. Engenheiros biomédicos com formação em aprendizado de máquina e processamento de sinais biomédicos têm acesso crescente a programas de mestrado e doutorado com bolsas FAPESP, CNPq e CAPES nessa área.
Perguntas Frequentes
O AIR Recon DL cardíaco já está disponível no Brasil?
A aprovação do FDA não implica disponibilidade imediata no mercado brasileiro. Para comercialização no Brasil, a GE HealthCare precisa submeter a atualização de software à ANVISA para inclusão no registro sanitário do equipamento SIGNA, seguindo a RDC nº 657/2022 para SaMD. O prazo estimado para registro de atualizações dessa natureza varia de 6 a 18 meses após a aprovação norte-americana, dependendo da estratégia regulatória adotada pelo fabricante e da complexidade da documentação técnica.
O sistema MAGNUS é compatível com equipamentos SIGNA já instalados?
Não. O sistema MAGNUS exige substituição completa do conjunto de bobinas de gradiente, amplificadores de gradiente e componentes estruturais relacionados, uma intervenção de hardware de grande porte que na prática equivale à instalação de um novo sistema. O MAGNUS é comercializado como equipamento novo, não como upgrade de campo. Isso o diferencia do AIR Recon DL cardíaco e do NeuroQuant integrado, ambos distribuídos como atualizações de software para sistemas SIGNA compatíveis já instalados.
Qual é a diferença entre o NeuroQuant integrado ao SIGNA e o software standalone anterior?
O NeuroQuant standalone exigia que o técnico de RM exportasse manualmente as imagens T1 3D em formato DICOM para um servidor separado, aguardasse o processamento remoto e importasse o relatório de volta ao PACS. O NeuroQuant integrado ao SIGNA realiza todo esse processo automaticamente ao fim da sequência MPRAGE, sem intervenção do técnico e sem necessidade de servidor externo. O resultado está disponível no PACS em 8 a 10 minutos após o término da aquisição, uma diferença de workflow relevante para a rotina clínica de alta demanda.
As aprovações do FDA para a plataforma SIGNA afetam a competitividade com a Siemens e a Philips no Brasil?
Sim, especialmente no segmento de alta complexidade. A aprovação do MAGNUS posiciona a GE HealthCare como única fabricante com sistema de gradientes de 200 mT/m aprovado para uso clínico, criando diferencial para centros acadêmicos e de pesquisa clínica avançada. No segmento de RM clínica convencional, a competição entre as três fabricantes continua intensa, com a Siemens Healthineers e a Philips também investindo em algoritmos de DL (Deep Resolve e SmartSpeed, respectivamente) com desempenho documentado em publicações peer-reviewed comparáveis ao AIR Recon DL.
O que as aprovações representam para estudantes de engenharia biomédica no Brasil?
As aprovações sinalizam três tendências concretas para o mercado de trabalho: a convergência entre aprendizado de máquina e engenharia de dispositivos médicos é irreversível e demanda formação híbrida em física da RM, processamento de sinais e redes neurais; a regulamentação de software como dispositivo médico (SaMD) é área em rápida expansão com escassez de profissionais qualificados; e o ciclo de inovação em equipamentos de RM está se acelerando, com aprovações de novas funcionalidades ocorrendo em prazos progressivamente menores, o que aumenta a demanda por profissionais capazes de implementar e validar tecnologias emergentes em ambiente clínico.
Volte ao Guia Definitivo de Engenharia Biomédica para explorar todas as seções.
Publicado por engenhariabiomedica.com
Artigos relacionados
Cirurgia Robótica no Brasil: 417% de Crescimento e o Papel do Engenheiro Biomédico
De 2 robôs em 2008 a 200 plataformas em 2025, o Brasil realizou 120 mil procedimentos robóticos acumulados e se tornou o 9º mercado mundial. Entenda o ecossistema de plataformas, regulamentação ANVISA/CFM, financiamento ANS e como o engenheiro biomédico é peça central nessa revolução.
Healthtechs Brasileiras: Mapa Completo do Ecossistema com 1.900+ Startups [2026]
O ecossistema de healthtechs Brasil reúne 1.900+ startups, movimenta US$ 6,34 bilhões e concentra 64,8% do investimento em saúde digital da América Latina.
Inteligência Artificial na Saúde Brasileira: O Mapa Completo para Engenheiros Biomédicos [2026]
Panorama completo da inteligência artificial na saúde brasileira em 2026: dados, regulação, mercado e oportunidades para engenheiros biomédicos.
Informática em Saúde: HIS, Prontuário Eletrônico e Interoperabilidade FHIR/HL7 [2026]
Guia completo sobre informática em saúde: HIS, prontuário eletrônico do paciente, padrões HL7 e FHIR, interoperabilidade, RNDS, mercado brasileiro e carreira para engenheiros biomédicos.