A IEC 60601 é a família de normas internacionais que define os requisitos de segurança e desempenho essencial para equipamentos eletromédicos. Com mais de 90 documentos normativos desenvolvidos pelo Comitê Técnico 62 (TC 62) da IEC, ela representa o principal framework regulatório para engenheiros de design que precisam certificar produtos e para engenheiros clínicos que avaliam a conformidade de equipamentos já em uso. Conhecer sua estrutura, seus conceitos fundamentais e os processos de ensaio exigidos não é opcional, é um requisito de competência profissional.
Se você está iniciando a jornada de certificação de um equipamento médico no Brasil, recomendamos também a leitura do nosso guia sobre certificação INMETRO para equipamentos médicos e sobre registro na ANVISA em 2026 que contextualizam o processo regulatório completo no qual a IEC 60601 se insere.
Histórico e Evolução: De 1977 à Edição 3.2
O TC 62 foi criado em 1967, e a primeira edição da IEC 60601-1 foi publicada em 1977, estabelecendo requisitos elétricos básicos para equipamentos médicos. A segunda edição, de 1988, expandiu o escopo e introduziu conceitos de classificação que ainda persistem. A grande virada aconteceu com a terceira edição, publicada em 2005: a norma abandonou a abordagem prescritiva pura e adotou um paradigma baseado em gerenciamento de risco, exigindo integração com a ISO 14971.
A edição atual é a 3.2 (2020), que incorporou emendas significativas. As principais mudanças em relação à Ed. 3.1 incluem a substituição da IEC 60950-1 pela IEC 62368-1 para avaliação de componentes fora do ambiente do paciente (MOOP), novos requisitos para baterias de lítio e limites térmicos atualizados para superfícies acessíveis. A FDA reconheceu formalmente a Ed. 3.2 em maio de 2022, tornando-a mandatória para novos pedidos de submissão a partir de dezembro de 2023.
A Emenda 2 (2020) da IEC 60601-1 trouxe 78 alterações aprovadas por maioria de dois terços dos comitês nacionais, incluindo substituição de referências normativas e novos requisitos para baterias de lítio e limites térmicos de contato.
— IEC TC 62, IEC 60601-1:2005/AMD2:2020, 2020
| Edição | Ano | Principal Característica |
|---|---|---|
| 1ª Edição | 1977 | Requisitos elétricos prescritivos básicos |
| 2ª Edição | 1988 | Classificação de partes aplicadas e expansão de escopo |
| 3ª Edição | 2005 | Paradigma baseado em risco (integração ISO 14971) |
| Ed. 3.1 | 2012 | Emenda com novos requisitos de usabilidade e alarmes |
| Ed. 3.2 | 2020 | IEC 62368-1 para MOOP, baterias Li-ion, limites térmicos atualizados |
A Arquitetura da IEC 60601: O Modelo Sanduíche
Descrição completa da imagem
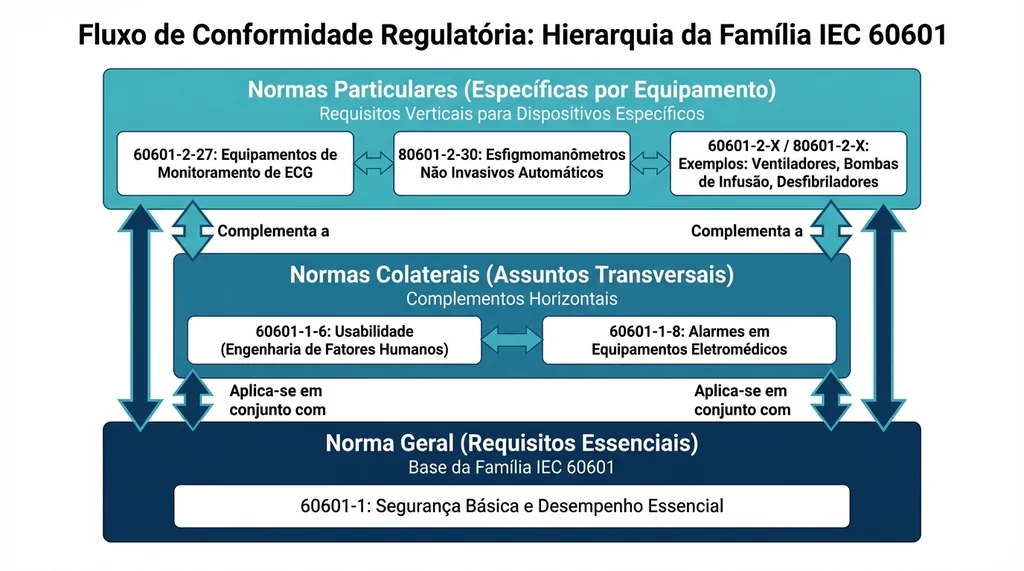
Diagrama hierárquico do modelo sanduíche da IEC 60601 com norma geral, colaterais e particulares em três camadas sobrepostas.
A família IEC 60601 organiza-se em um modelo hierárquico de três camadas, frequentemente chamado de modelo sanduíche. Compreender essa estrutura é fundamental antes de qualquer projeto de certificação.
Norma Geral: IEC 60601-1
A base do modelo é a IEC 60601-1 que estabelece os requisitos gerais de segurança básica e desempenho essencial aplicáveis a todos os equipamentos eletromédicos. Ela define conceitos fundamentais como ambiente do paciente, MOPP, MOOP, classificação de partes aplicadas e a obrigação de manutenção de um arquivo de gerenciamento de risco. Aproximadamente 140 de seus itens remetem explicitamente a evidências do processo de gerenciamento de risco conforme a ISO 14971.
Normas Colaterais: IEC 60601-1-X
Sobre a norma geral, aplicam-se as normas colaterais que tratam de aspectos transversais presentes em múltiplas categorias de equipamentos. Existem oito normas colaterais ativas:
- IEC 60601-1-2: Compatibilidade eletromagnética (EMC)
- IEC 60601-1-3: Proteção contra radiação em equipamentos de diagnóstico por raios X
- IEC 60601-1-6: Usabilidade
- IEC 60601-1-8: Sistemas de alarme
- IEC 60601-1-9: Ecodesign (redução de impacto ambiental)
- IEC 60601-1-10: Controladores em malha fechada fisiológica
- IEC 60601-1-11: Uso em ambientes de cuidados domiciliares
- IEC 60601-1-12: Uso em ambientes de emergência pré-hospitalar
Normas Particulares: IEC 60601-2-X e IEC 80601-2-X
No topo do sanduíche estão as normas particulares que tratam de tipos específicos de equipamentos. Existem mais de 60 normas particulares publicadas, cobrindo desde monitores de ECG (60601-2-27) até ventiladores (80601-2-12) e equipamentos de ressonância magnética (60601-2-33). Quando existe uma norma particular aplicável ao produto, ela prevalece sobre a norma geral nos pontos em que houver conflito, pois reflete requisitos específicos do contexto clínico daquele equipamento.
Para equipamentos presentes em UTIs, como monitores multiparamétricos e ventiladores, recomendamos a leitura do nosso guia sobre equipamentos de UTI que discute quais normas particulares são mais frequentemente exigidas nesses ambientes.
Conceitos Fundamentais: O Vocabulário da Norma
Antes de avançar para os ensaios e requisitos, é necessário dominar os conceitos que estruturam a lógica da norma.
Segurança Básica e Desempenho Essencial
A segurança básica refere-se à ausência de riscos inaceitáveis causados diretamente por perigos físicos, choque elétrico, calor excessivo, radiação mecânica ou eletromagnética. Já o desempenho essencial é a função clínica cuja falha ou degradação pode resultar em risco inaceitável ao paciente, operador ou terceiros. Por exemplo, para um desfibrilador, a capacidade de entregar a energia programada é desempenho essencial; para um oxímetro de pulso, é a precisão da leitura de SpO₂. O fabricante é responsável por identificar e declarar o desempenho essencial de seu equipamento no processo de gerenciamento de risco.
MOPP e MOOP
Dois conceitos de isolamento são centrais na IEC 60601:
- MOPP (Means of Patient Protection): Meio de proteção aplicado entre partes que podem tocar o paciente e a rede elétrica. Os requisitos são mais rigorosos, pois consideram a resistência reduzida do paciente em situação clínica (pele úmida, eletrodos internos etc.). Um isolamento pode ser classificado como 1 MOPP ou 2 MOPP dependendo da rigidez dielétrica e distâncias de escoamento exigidas.
- MOOP (Means of Operator Protection): Meio de proteção aplicado em partes acessíveis apenas ao operador, fora do ambiente do paciente. Com a Ed. 3.2, os requisitos de MOOP foram alinhados à IEC 62368-1, resultando em alterações nos valores de tensão de ensaio e distâncias mínimas.
Ambiente do Paciente
A norma define o ambiente do paciente como a região delimitada por uma distância de 1,83 m ao redor do local onde o paciente normalmente se encontra. Qualquer parte condutiva dentro dessa área que possa entrar em contato com o paciente deve ser classificada e isolada como parte aplicada. Essa delimitação espacial é determinante para identificar quais componentes do equipamento estão sujeitos aos requisitos mais restritivos de MOPP.
Classificação de Partes Aplicadas: Type B, BF e CF
Descrição completa da imagem
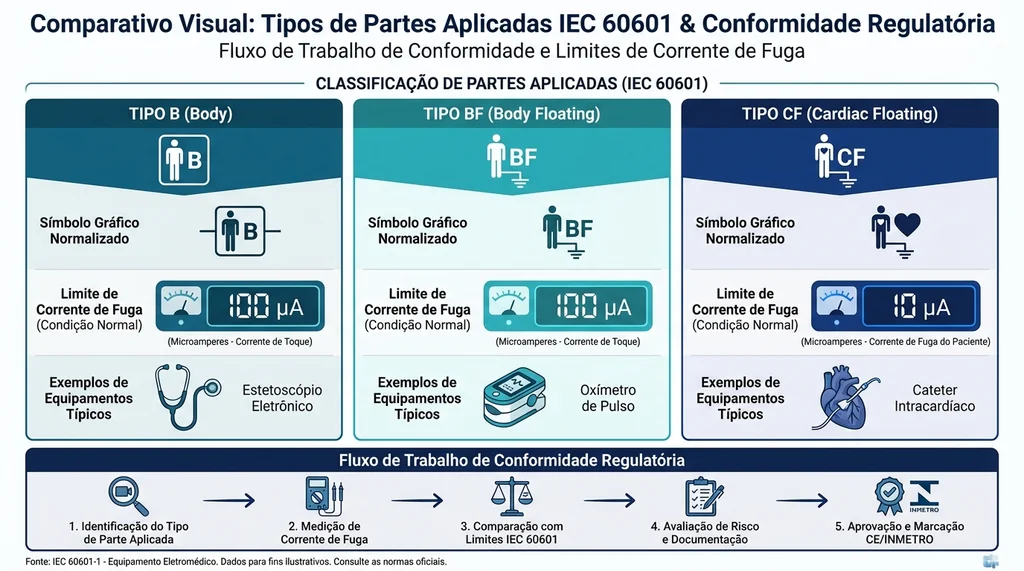
Tabela comparativa dos tipos de partes aplicadas IEC 60601 mostrando símbolos B, BF e CF com limites de corrente de fuga e exemplos de uso clínico.
As partes aplicadas são os elementos do equipamento destinados a entrar em contato físico com o paciente para a realização da função clínica. Elas são classificadas em três tipos com base no nível de proteção contra choque elétrico e no contexto de aplicação:
| Tipo | Símbolo | Corrente de Fuga Máx. (Normal) | Aplicação Típica |
|---|---|---|---|
| Type B | B | 100 µA | Contato externo não intencional (estetoscópio eletrônico) |
| Type BF | BF (com quadro) | 100 µA | Contato externo intencional isolado (eletrodos de ECG, oxímetro) |
| Type CF | CF (com coração) | 10 µA | Aplicação direta ao coração (cateteres intracardíacos, marca-passos) |
A distinção entre BF e CF é crítica: enquanto o tipo BF é adequado para aplicações no tronco externo ou membros, apenas o tipo CF pode ser usado em contato direto com o coração, pois o coração é especialmente sensível a microchoque, correntes tão baixas quanto 10 µA podem induzir fibrilação ventricular quando aplicadas diretamente ao miocárdio.
A família IEC 60601 compreende aproximadamente 90 a 95 documentos normativos ativos, com crescimento contínuo à medida que novas tecnologias como robótica médica e terapia a plasma geram novos padrões particulares.
— IEC TC 62, Catálogo de Normas IEC 60601, 2025
A classificação elétrica quanto à proteção contra choque segue outro eixo: Classe I (equipamentos com aterramento de proteção) e Classe II (equipamentos com isolamento duplo ou reforçado, sem dependência de aterramento). Equipamentos de Classe II são frequentemente preferidos em ambientes domiciliares ou portáteis, onde a integridade do aterramento não pode ser garantida.
As Normas Colaterais em Detalhe
IEC 60601-1-2: Compatibilidade Eletromagnética
A norma colateral de EMC estabelece requisitos de emissão e imunidade para equipamentos eletromédicos. A edição 4 (2014, com emenda de 2020) trouxe uma abordagem baseada em risco para definir os requisitos de imunidade: o fabricante deve avaliar, dentro do processo da ISO 14971, quais distúrbios eletromagnéticos são plausíveis no ambiente de uso pretendido e dimensionar os requisitos de imunidade correspondentes. Ambientes de saúde especializados (como sala de cateterismo com fluoroscopia) têm requisitos de imunidade mais elevados do que ambientes de atenção básica.
A Emenda 1 da IEC 60601-1-2 (2020) adicionou ensaios de imunidade a campos magnéticos de proximidade conforme IEC 61000-4-39 e atualizou requisitos para comunicações RF sem fio, incluindo WiFi, Bluetooth e 5G.
— IEC SC 62A, IEC 60601-1-2:2014/AMD1:2020, 2020
IEC 60601-1-6: Usabilidade
Esta norma colateral exige que o fabricante conduza um processo de engenharia de usabilidade que inclua análise de uso, estudos formativos e estudos de validação sumativa com usuários representativos. O vínculo com a IEC 62366-1 é direto, a 60601-1-6 referencia essa norma para os detalhes do processo. Erros de uso são considerados como perigos potenciais no gerenciamento de risco, e a interface do equipamento deve ser projetada para minimizá-los.
IEC 60601-1-8: Sistemas de Alarme
Alarmes são um ponto crítico em equipamentos de monitoração e terapia. A IEC 60601-1-8 define três níveis de prioridade (alta, média, baixa), requisitos acústicos para tons de alarme, requisitos visuais para indicadores e obrigações relacionadas à configuração e desativação de alarmes. Para engenheiros clínicos que gerenciam ambientes de UTI, conhecer esta norma é fundamental para avaliar a adequação dos sistemas de alarme de equipamentos adquiridos, tema aprofundado em nosso guia sobre equipamentos de UTI.
Ensaios de Segurança: O Que os Laboratórios Verificam

A conformidade com a IEC 60601 é demonstrada por meio de ensaios realizados por laboratórios acreditados. Os principais grupos de ensaios são:
Ensaios de Segurança Elétrica
Os ensaios elétricos verificam correntes de fuga, resistência de aterramento, rigidez dielétrica e continuidade do condutor de proteção. As correntes de fuga avaliadas incluem:
- Corrente de fuga ao terra (earth leakage): corrente que flui pelo condutor de proteção em condições normais e de primeira falha
- Corrente de fuga do invólucro (enclosure leakage): corrente entre o invólucro e o terra em superfícies acessíveis
- Corrente de fuga de parte aplicada (patient leakage): corrente entre partes aplicadas e terra, no sentido para o paciente ou no sentido inverso
- Corrente auxiliar de paciente (patient auxiliary current): corrente entre partes aplicadas que circula pelo paciente sem função terapêutica pretendida
Os ensaios são realizados em condição normal e em condição de primeira falha que simula situações como interrupção do condutor de proteção ou falha de um componente de isolamento. Os limites são mais permissivos em condição normal e mais restritivos em primeira falha, diferentemente de outras normas de segurança elétrica, a IEC 60601 exige que o equipamento permaneça seguro mesmo com uma falha única.
Ensaios de EMC
Os ensaios de EMC incluem tanto a verificação de emissão conduzida e irradiada (para garantir que o equipamento não interfira em outros) quanto a verificação de imunidade a distúrbios típicos do ambiente hospitalar: descargas eletrostáticas, campos eletromagnéticos irradiados, transientes elétricos rápidos, surtos e variações de tensão na rede.
Ensaios Mecânicos e Ambientais
Incluem testes de resistência mecânica, queda, vibração, pressão de contato e temperatura de superfícies acessíveis. Com a Ed. 3.2, os limites térmicos de superfícies acessíveis foram revisados, com valores diferenciados para superfícies de contato intencional (como manoplas) e não-intencional, e com consideração de diferentes materiais (metal, plástico, cerâmica).
Ensaios de Desempenho Essencial
Esses ensaios verificam se o equipamento mantém seu desempenho essencial declarado mesmo na presença de distúrbios (EMC, falhas de alimentação, condições ambientais extremas). A definição e o protocolo de ensaio do desempenho essencial são responsabilidade do fabricante e devem estar documentados no arquivo de gerenciamento de risco.
| Grupo de Ensaios | Normas de Referência | Principal Verificação |
|---|---|---|
| Segurança Elétrica | IEC 60601-1 (Cláusulas 8, 16, 17) | Correntes de fuga, rigidez dielétrica, aterramento |
| EMC | IEC 60601-1-2 Ed. 4 | Emissão conduzida/irradiada, imunidade |
| Mecânico/Ambiental | IEC 60601-1 (Cláusulas 9, 11, 12) | Resistência mecânica, temperatura, IP |
| Desempenho Essencial | 60601-1 + Norma Particular | Função clínica sob perturbação |
| Alarmes | IEC 60601-1-8 | Acústica, visual, prioridades, desativação |
IEC 60601 no Brasil: ABNT NBR e Regulamentação ANVISA/INMETRO
No Brasil, a família IEC 60601 é adotada como ABNT NBR IEC 60601 com tradução oficial das normas internacionais. A adoção não é automática, cada norma internacional passa por processo de votação e publicação como norma brasileira, o que pode gerar defasagem temporal entre a edição IEC e a versão ABNT disponível.
Para fins de certificação compulsória pelo INMETRO, a Portaria 384/2020 lista as categorias de equipamentos eletromédicos sujeitos a certificação obrigatória e as normas aplicáveis. A conformidade com a série ABNT NBR IEC 60601 é exigida para obtenção do certificado, que é pré-requisito para o registro ou cadastro na ANVISA.
A IN ANVISA 283/2024 atualiza a lista de normas de desempenho e segurança que devem ser observadas no âmbito do registro de dispositivos médicos, incluindo referências explícitas à série IEC 60601. Mais detalhes sobre o processo de certificação INMETRO estão em nosso artigo dedicado sobre certificação INMETRO para equipamentos médicos.
Para equipamentos importados com certificação IEC 60601-1 Ed. 3.2 obtida em laboratórios reconhecidos por esquemas como IECEE CB Scheme, é possível aproveitar o relatório de ensaio internacional para reduzir o escopo dos ensaios nacionais, prática conhecida como reconhecimento mútuo de resultados de ensaio.
Integração com a ISO 14971: Gestão de Risco como Espinha Dorsal
A Ed. 3 da IEC 60601-1 transformou o processo de gestão de risco conforme a ISO 14971 de uma boa prática em um requisito normativo explícito. Aproximadamente 140 cláusulas da norma remetem ao arquivo de gerenciamento de risco como evidência de conformidade.
Isso significa que a análise de risco não é um documento separado e opcional, ela é a argumentação central que justifica as decisões de design. Para cada perigo identificado (choque elétrico, superaquecimento, falha de alarme, interferência eletromagnética), o fabricante deve demonstrar que os riscos residuais são aceitáveis após as medidas de controle implementadas, sejam elas inerentes ao design, protetoras ou informativas.
A integração com o sistema de gestão de qualidade ISO 13485 é igualmente importante: os registros do processo de gestão de risco devem ser mantidos como documentos controlados dentro do SGQ, com rastreabilidade entre versões de produto, versões de norma e revisões de risco.
Aplicação em Equipamentos de Centro Cirúrgico
Equipamentos utilizados em centros cirúrgicos, como bisturis elétricos, sistemas de videolaparoscopia, bombas de infusão e monitores hemodinâmicos, estão sujeitos a requisitos ainda mais específicos. Além das normas particulares aplicáveis a cada tipo de equipamento, o ambiente cirúrgico levanta questões adicionais relacionadas ao uso em ambientes com gases anestésicos (requisitos AP e APG, que restringem o uso de arcos elétricos) e ao uso de múltiplos equipamentos conectados simultaneamente ao mesmo paciente (o que exige avaliação da corrente de fuga cumulativa em sistemas eletromédicos, IEC 60601-1 Cláusula 16 e Anexo B). Nosso guia sobre equipamentos de centro cirúrgico aprofunda esses aspectos.
Recursos Externos e Referências Normativas
Para acesso às normas e documentos regulatórios relacionados, os seguintes recursos oficiais são essenciais:
- IEC TC 62, Comitê Técnico de Equipamentos Elétricos em Medicina: página oficial com escopo do comitê e lista de normas publicadas
- FDA, Recognized Consensus Standards: banco de dados atualizado de normas reconhecidas pela FDA, incluindo a IEC 60601-1 Ed. 3.2
- ABNT, Associação Brasileira de Normas Técnicas: catálogo de normas brasileiras, incluindo a série ABNT NBR IEC 60601
Perguntas Frequentes sobre a IEC 60601
A IEC 60601-1 Ed. 3.2 substitui completamente a Ed. 3.1?
Sim. A Ed. 3.2 (2020) é uma edição consolidada que incorpora as emendas 1 e 2 à Ed. 3 (2005), substituindo tanto a Ed. 3.0 quanto a Ed. 3.1. Para novos projetos de certificação, deve-se sempre utilizar a edição mais recente reconhecida pela autoridade regulatória do mercado-alvo. No caso da FDA, a Ed. 3.2 tornou-se obrigatória para novas submissões a partir de dezembro de 2023.
Todo equipamento eletromédico precisa ter uma norma particular aplicável?
Não. A existência de uma norma particular é desejável, mas não obrigatória para a certificação. Quando não existe norma particular para o tipo de equipamento, a conformidade é demonstrada exclusivamente com base na IEC 60601-1 e nas normas colaterais pertinentes. Nesses casos, o processo de gerenciamento de risco ganha ainda mais importância, pois é o mecanismo pelo qual o fabricante justifica as decisões de design na ausência de requisitos particulares pré-definidos.
Qual é a diferença entre "segurança básica" e "desempenho essencial" na prática?
Segurança básica é o conjunto de proteções que previnem danos físicos diretos decorrentes do equipamento, choque elétrico, queimadura, explosão. Desempenho essencial é a função clínica que, se degradada ou perdida, pode colocar o paciente em risco, mesmo sem qualquer dano físico direto causado pelo equipamento em si. Um monitor de pressão arterial que subitamente para de exibir leituras não causa choque elétrico, mas a falha no desempenho essencial pode levar a uma decisão clínica errada. Ambos os aspectos devem ser demonstrados nos ensaios de conformidade.
O IECEE CB Scheme facilita a certificação no Brasil?
O IECEE CB Scheme é um acordo de reconhecimento mútuo de resultados de ensaio entre organismos de certificação de mais de 50 países. No Brasil, o INMETRO participa do esquema por meio de laboratórios designados. Um relatório CB obtido em laboratório acreditado pode ser utilizado como base para a certificação nacional, potencialmente reduzindo o escopo dos ensaios adicionais exigidos. No entanto, diferenças de desvios nacionais (national deviations) devem ser avaliadas caso a caso, e o INMETRO pode exigir ensaios complementares.
Como a IEC 60601-1-11 afeta equipamentos para uso domiciliar?
A norma colateral 60601-1-11 (uso em ambientes de cuidados domiciliares) impõe requisitos adicionais importantes: os equipamentos devem ser projetados para operar com usuários não profissionais, em ambientes com variabilidade maior de condições ambientais (temperatura, umidade), com redes elétricas potencialmente de menor qualidade e sem a supervisão contínua de profissionais de saúde. Isso se traduz em requisitos de usabilidade mais rigorosos (instruções de uso simplificadas, menor probabilidade de erro de configuração), robustez mecânica aumentada e faixas de operação ambiental mais amplas.
Artigos relacionados
ANVISA e Dispositivos Médicos: Guia Completo de Regulamentação [Atualizado 2026]
Guia completo sobre regulamentação de dispositivos médicos pela ANVISA: classes de risco I-IV, fluxo de registro, documentação exigida, prazos, custos e as principais RDCs de 2022 a 2025. Conteúdo atualizado para profissionais de regulatory affairs, startups e fabricantes.
Certificação INMETRO para Equipamentos Médicos: Processo Passo a Passo
Guia completo sobre a certificação INMETRO de equipamentos eletromédicos no Brasil: Portaria 384/2020, normas IEC 60601, laboratórios acreditados, custos, prazos e o processo detalhado passo a passo para fabricantes e importadores.
Como Registrar um Dispositivo Médico na ANVISA: Roteiro Prático para Startups e Fabricantes
Guia completo do processo de registro de dispositivos médicos na ANVISA: classificação, CBPF, ensaios técnicos, submissão no sistema SOLICITA e acompanhamento. Prazos reais, custos atualizados e erros mais comuns a evitar.
ISO 13485 para Dispositivos Médicos: Implementação Prática do Sistema de Gestão da Qualidade
Guia completo de implementação da ISO 13485:2016 com checklists por cláusula, templates de procedimentos, custos reais de certificação e estratégias para auditoria. Essencial para gestores de qualidade e consultores do setor de dispositivos médicos no Brasil.