A compra de equipamentos hospitalares no Brasil envolve um dos processos burocráticos mais complexos da administração pública, e os erros cometidos na fase de especificação técnica ou na elaboração do edital podem resultar em aquisições inadequadas, impugnações, superfaturamento ou equipamentos inoperantes por falta de acessórios e suporte. Com a entrada em vigor da Lei 14.133/2021 como marco jurídico obrigatório a partir de 30 de dezembro de 2023, hospitais públicos, secretarias de saúde e fundações hospitalares precisaram se adaptar a uma nova lógica de contratação, mais planejada, mais transparente e com o engenheiro clínico no centro do processo técnico.
Este artigo integra o ecossistema de conteúdo sobre gestão tecnológica hospitalar do portal, complementando diretamente os artigos sobre Gestão de Parque Tecnológico Hospitalar Manutenção de Equipamentos Hospitalares Equipamentos de Diagnóstico por Imagem e Equipamentos de UTI. Se você atua em engenharia clínica, gestão hospitalar ou no setor de empresas de dispositivos médicos no Brasil este guia oferece o mapa completo do processo de aquisição.
A Nova Lei de Licitações (14.133/2021) e o Impacto nas Compras Hospitalares
A Lei 14.133/2021, conhecida como Nova Lei de Licitações e Contratos Administrativos, revogou definitivamente em 30 de dezembro de 2023 a Lei 8.666/1993, que havia regulamentado as compras públicas brasileiras por três décadas. Para a área de saúde, a transição representou uma mudança estrutural: o novo marco legal incorporou boas práticas de contratação pública reconhecidas internacionalmente e tornou obrigatório o planejamento da contratação como fase autônoma e documentada.
Os principais impactos da Lei 14.133/2021 para compras hospitalares são:
- Estudo Técnico Preliminar (ETP) obrigatório: toda contratação relevante deve ser precedida de um ETP que demonstre a necessidade, as alternativas avaliadas e a solução técnica escolhida.
- Gerenciamento de Riscos formal: a fase de planejamento inclui a identificação e mitigação de riscos contratuais, com matriz de riscos documentada.
- Cinco modalidades licitatórias: pregão eletrônico, concorrência, diálogo competitivo, credenciamento e leilão, extinguindo a tomada de preços e o convite da lei anterior.
- Diálogo Competitivo como novidade: modalidade inédita no Brasil, voltada para contratações inovadoras onde a administração não consegue definir sozinha a solução técnica.
- Publicação obrigatória no PNCP: o Portal Nacional de Contratações Públicas tornou-se o repositório oficial de todos os editais, contratos e atas de registro de preços públicos.
| Modalidade | Aplicação em Equipamentos Hospitalares | Critério de Julgamento | Ambiente |
|---|---|---|---|
| Pregão Eletrônico | Equipamentos padronizados: monitores, bombas de infusão, desfibriladores | Menor preço ou maior desconto | Plataformas ComprasNet, BLL, Licitanet |
| Concorrência | Equipamentos de alta complexidade: RM, acelerador linear, PET-CT | Menor preço, técnica e preço ou melhor técnica | Eletrônico ou presencial |
| Diálogo Competitivo | Tecnologias inovadoras sem especificação consolidada, soluções integradas | Técnica e preço | Sessões de diálogo presenciais |
| Credenciamento | Prestadores de manutenção, suporte técnico especializado | Critérios de habilitação técnica | Contínuo, sem disputa |
| Dispensa de Licitação | Emergências, valores abaixo de R$ 57.490 (obras) / R$ 28.745 (bens) | Cotação mínima de três fornecedores | Eletrônico obrigatório acima de R$ 10.000 |

O Estudo Técnico Preliminar (ETP): Documento Fundacional da Compra
O Estudo Técnico Preliminar é o coração do planejamento de contratação sob a Lei 14.133/2021. Para equipamentos hospitalares, ele deve responder rigorosamente a um conjunto de perguntas técnicas antes que qualquer edital seja elaborado. O ETP mal feito é a causa raiz de mais de 60% dos problemas em licitações hospitalares, especificações inadequadas, itens ausentes, incompatibilidades com infraestrutura existente e aquisição de equipamentos sem suporte técnico disponível no Brasil.
Um ETP completo para equipamentos médicos deve conter:
- Descrição da necessidade: justificativa clínica, epidemiológica ou operacional com dados quantitativos (demanda de exames, capacidade instalada atual, taxa de falha do equipamento substituído).
- Levantamento de mercado: mapeamento de fornecedores com registro ANVISA, visitas técnicas, análise de soluções disponíveis e benchmarking com outras instituições.
- Análise de alternativas: avaliação de compra versus comodato, equipamento novo versus remanufaturado, aquisição direta versus registro de preços.
- Estimativa de custo total de propriedade (TCO): custo de aquisição + manutenção ao longo da vida útil + insumos + treinamento + descarte, não apenas o preço de compra.
- Requisitos de infraestrutura: carga elétrica, aterramento, climatização, blindagem, canalização de gases, área mínima e resistência de piso.
- Declaração de viabilidade: confirmação técnica, orçamentária e jurídica da contratação pretendida.
Como Elaborar a Especificação Técnica Sem Direcionamento de Marca
A especificação técnica de equipamentos médicos é onde o engenheiro clínico tem o papel mais crítico e mais delicado do processo. A lei proíbe o direcionamento para marcas ou fabricantes específicos, mas exige ao mesmo tempo especificações suficientemente precisas para garantir que o equipamento adquirido atenda à necessidade clínica real. Esse equilíbrio é difícil e violado com frequência.
A especificação por função ou desempenho é a abordagem correta: em vez de citar "ventilador mecânico Marca X modelo Y", o edital deve descrever os parâmetros funcionais que qualquer equipamento equivalente deve cumprir, pressão de trabalho, modos ventilatórios, interface, alarmes, conectividade e compatibilidade com infraestrutura existente.
Diretrizes práticas para especificação técnica legal e eficaz:
- Descreva parâmetros mínimos de desempenho com valores verificáveis, faixas numéricas, não marcas.
- Inclua normas técnicas aplicáveis: IEC 60601-1, IEC 60601-2-X da série específica do equipamento, ABNT NBR equivalentes.
- Exija registro na ANVISA como condição de habilitação, não como especificação técnica, para não direcionar para número de registro específico.
- Quando citar marca como referência for inevitável (infraestrutura já instalada), adicione a cláusula "ou equivalente superior" com critérios objetivos de equivalência definidos.
- Documente no ETP a justificativa técnica de cada requisito especificado, qualquer restrição de mercado precisa ter embasamento técnico auditável.
- Evite especificações que só um fabricante atende sem justificativa técnica, o TCU pode anular o processo por restrição indevida à competitividade.
A Operação Ressonância do TCU (Acórdão 1290/2018-Plenário) revelou superfaturamento de R$ 86 milhões em 9 pregões do INTO no Rio de Janeiro, com direcionamento sistêmico, simulação de competição e uso indevido de pregão presencial.
— Tribunal de Contas da União, Acórdão 1290/2018-Plenário
| Prática | Correto | Incorreto (Direcionamento) |
|---|---|---|
| Identificação de marca | "Equipamento de RX digital, sistema flat-panel, resolução mínima 3 Lp/mm" | "Equipamento de RX digital modelo Definium da GE Healthcare" |
| Referência a software | "Software com compatibilidade DICOM 3.0 e integração HL7 v2.x" | "Software Centricity ou equivalente" |
| Norma técnica | "Conforme IEC 60601-2-37 para equipamentos de ultrassom" | "Conforme certificado emitido pelo INMETRO sob portaria XX" |
| Acessórios | "Eletrodos de superfície compatíveis com conector padrão DIN 42802" | "Eletrodos originais do fabricante do monitor" |

Verificação de Registro ANVISA e Certificação INMETRO
Dois requisitos regulatórios são inegociáveis em qualquer compra de equipamento médico no Brasil e devem ser verificados antes da habilitação dos licitantes, nunca apenas no momento da entrega.
Registro ANVISA: todo produto de saúde comercializado no Brasil precisa ter registro, cadastro ou notificação ativa junto à ANVISA, conforme a classe de risco determinada pela RDC 751/2021 (que substituiu a RDC 185/2001). A verificação deve ser feita diretamente no Consultas ANVISA pelo número de CNPJ da empresa detentora do registro, não pelo número de registro informado pelo fornecedor, para confirmar que o registro está ativo, que o produto especificado está incluído no escopo do registro e que o CNPJ declarado é o correto.
Certificação INMETRO: equipamentos elétricos médicos de alta tensão (radiologia, tomografia, radioterapia) e alguns dispositivos específicos são objeto de certificação compulsória pelo INMETRO via portarias específicas. O edital deve exigir o certificado de conformidade emitido por Organismo de Certificação de Produto (OCP) acreditado pelo INMETRO, e a comissão de avaliação deve verificar o prazo de validade do certificado e o escopo exato de certificação.
Análise de Custo Total de Propriedade (TCO) em Equipamentos Médicos
O custo de aquisição representa tipicamente apenas 20 a 30% do custo total de propriedade (TCO) de um equipamento hospitalar ao longo de sua vida útil de 10 anos. Um tomógrafo adquirido por R$ 3 milhões pode gerar TCO de R$ 8 a 12 milhões.
— Análise de Custo Total de Propriedade, IN SEGES nº 58/2022
O preço de aquisição de um equipamento médico representa, em média, apenas 30 a 40% do custo total gerado ao longo de sua vida útil. Ignorar os custos de ciclo de vida é o erro mais frequente e mais caro nas compras hospitalares, e a principal causa de orçamentos de manutenção cronicamente insuficientes.
O TCO (Total Cost of Ownership) deve ser calculado para o horizonte temporal da vida útil esperada do equipamento, tipicamente 8 a 15 anos para equipamentos de diagnóstico por imagem, 7 a 10 anos para monitores e ventiladores, 5 a 7 anos para bombas de infusão, e incluir:
| Componente do TCO | Descrição | Participação Típica no TCO |
|---|---|---|
| Preço de aquisição | Valor do equipamento principal, incluindo acessórios e opcionais | 30–40% |
| Instalação e comissionamento | Obras de adaptação, instalação elétrica especial, blindagem, gases medicinais | 5–15% |
| Treinamento | Capacitação inicial de operadores e técnicos de manutenção | 1–3% |
| Manutenção preventiva | Contratos anuais de PM, calibração e qualificação de desempenho | 10–20% |
| Manutenção corretiva e peças | Reparos não programados, reposição de componentes, peças de alto desgaste | 10–20% |
| Insumos e consumíveis | Eletrodos, géis, filtros, tubos de raios X (no caso de TC), contrastes relacionados | 10–25% |
| Custo de energia elétrica | Consumo mensal ao longo da vida útil, relevante para TC, RM e aceleradores | 2–8% |
| Descarte e destinação final | Logística reversa, tratamento de resíduos especiais (radioativos, eletrônicos) | 1–3% |
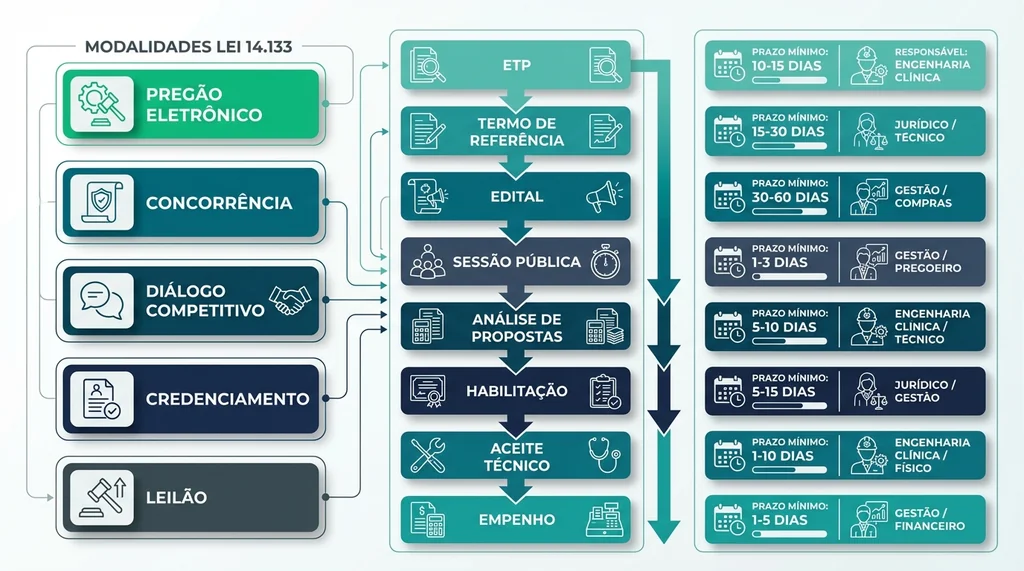
Descrição completa da imagem
Fluxograma técnico das modalidades licitatórias da Lei 14.133/2021 e etapas do processo de compra de equipamentos hospitalares do ETP ao aceite técnico.
Critérios de Avaliação Técnica: Matriz de Conformidade e Modelo de Pontuação
Em licitações de equipamentos de alta complexidade, onde o critério de julgamento é técnica e preço a comissão de avaliação utiliza instrumentos estruturados para pontuar as propostas recebidas. O engenheiro clínico é o profissional designado para liderar essa avaliação e assinar o parecer técnico.
A matriz de conformidade é o instrumento básico: uma tabela com todos os requisitos técnicos do edital, onde cada proposta recebe "conforme", "não conforme" ou "parcialmente conforme" para cada item. Propostas com itens essenciais não conformes são desclassificadas antes da fase de pontuação.
O modelo de pontuação (scoring model) é aplicado quando o edital prevê julgamento por melhor técnica: cada atributo técnico recebe um peso e uma escala de pontuação definidos no edital. Os atributos mais comuns em equipamentos médicos incluem:
- Conformidade com requisitos mínimos obrigatórios (binário, eliminatório)
- Desempenho técnico acima do mínimo especificado (pontuação proporcional)
- Capacidade de assistência técnica no Brasil, rede de serviço própria ou autorizada
- Disponibilidade de peças de reposição com prazo garantido em contrato
- Prazo de garantia superior ao mínimo exigido
- Certificações adicionais (ISO 13485, ISO 9001 do fabricante)
- Apresentação de atestados técnicos de fornecimento a hospitais de perfil equivalente
Requisitos de Pós-Venda, Garantia e Manutenção em Edital
A fase de uso e manutenção do equipamento começa a ser planejada no edital, não depois da entrega. Hospitais que não definem com precisão os requisitos de pós-venda no processo licitatório enfrentam contratos de manutenção leoninos, peças importadas com prazos de fornecimento de meses e fornecedores sem estrutura de campo no Brasil.
O edital de equipamentos médicos deve especificar obrigatoriamente:
- Garantia mínima: prazo (tipicamente 12 a 24 meses), cobertura (peças, mão de obra, deslocamento) e exclusões.
- Tempo de resposta (SLA): prazo máximo para o técnico comparecer ao local após chamado, geralmente 4 a 8 horas para equipamentos críticos, 24 a 48 horas para não críticos.
- Disponibilidade de peças: garantia contratual de fornecimento de peças por período determinado pós-venda, mínimo de 5 anos para equipamentos de alta complexidade.
- Treinamento inicial: carga horária mínima, perfil dos treinados (operadores, técnicos de manutenção), local de realização e fornecimento de material didático.
- Manual técnico completo em português: manual de operação, manual de serviço com esquemas elétricos e procedimentos de manutenção preventiva.
- Representante técnico no Brasil: exigência de que o fornecedor possua estrutura de suporte técnico própria ou autorizada com endereço no território nacional.
Em 2024, o total de emendas parlamentares alcançou R$ 44,67 bilhões, com 66% destinados à saúde — R$ 21,2 bilhões no Ministério da Saúde. Adicionalmente, o governo federal anunciou em agosto de 2025 investimento de R$ 2,4 bilhões em mais de 10 mil equipamentos de saúde.
— Ministério da Saúde / Lei Complementar 210/2024
Comodato versus Compra: Análise Decisória
O comodato modalidade em que o fornecedor cede o equipamento gratuitamente em troca do compromisso de compra exclusiva de insumos ou reagentes, é amplamente utilizado em laboratórios clínicos (analisadores hematológicos, bioquímicos, imunológicos) e em algumas áreas de diagnóstico por imagem. Para hospitais, a análise da melhor modalidade deve ser feita caso a caso no ETP.
A decisão entre comodato e compra deve considerar:
- Volume de consumo de insumos: o comodato é economicamente vantajoso apenas quando o volume de consumo do hospital justifica o preço por unidade de insumo cobrado pelo fornecedor, que embutiu o custo do equipamento nos insumos.
- Dependência de fornecedor único: o comodato cria lock-in tecnológico pelo período contratual, mudança de fornecedor implica troca de plataforma analítica e revalidação de métodos.
- Custos totais comparados: a análise financeira deve comparar o TCO da compra com o TCO do comodato (custo total dos insumos pelo período de vida útil previsto do equipamento).
- Risco de obsolescência: no comodato, o fornecedor frequentemente assume o risco de atualização tecnológica, vantagem relevante em áreas de evolução tecnológica acelerada.
- Enquadramento jurídico: comodatos na rede pública devem ser formalizados por contrato administrativo com chamamento público, não por mero acordo comercial.
Aceite Técnico: O Protocolo de Recebimento de Equipamentos
O aceite técnico (ou recebimento técnico definitivo) é o procedimento formal pelo qual o hospital atesta que o equipamento entregue cumpre integralmente as especificações do edital e está em perfeito estado de funcionamento. É a última linha de defesa antes de o contrato ser executado e o pagamento liberado, e precisa ser conduzido pelo engenheiro clínico com rigor metodológico.
Um protocolo de aceite técnico completo inclui:
- Conferência documental: registro ANVISA vigente, certificado INMETRO (se aplicável), manual técnico em português, certificado de calibração dos instrumentos utilizados na instalação.
- Conferência de itens fornecidos: checklist contra a proposta vencedora, equipamento principal, acessórios, consumíveis iniciais, softwares com licenças, cabos e periféricos.
- Testes de desempenho: verificação instrumental dos parâmetros críticos especificados no edital, usando equipamentos padrão calibrados rastreáveis ao INMETRO/RBC.
- Inspeção de segurança elétrica: conforme IEC 60601-1, resistência de aterramento, corrente de fuga, rigidez dielétrica.
- Verificação de alarmes: teste funcional de todos os alarmes especificados.
- Registro fotográfico: documentação fotográfica do equipamento instalado, número de série, plaqueta de identificação e estado geral.
- Treinamento antes do aceite: certificar que o treinamento dos operadores foi realizado conforme contratado antes de emitir o aceite técnico definitivo.
O aceite deve ser formalizado em termo assinado pelo engenheiro clínico responsável, pelo representante do fornecedor e pelo gestor do contrato, e arquivado como documento de gestão do ciclo de vida do equipamento no sistema de gerenciamento do parque tecnológico.
Financiamento de Equipamentos Hospitalares no SUS
Para hospitais e redes públicas de saúde, a compra de equipamentos pode contar com mecanismos de financiamento federal que reduzem o impacto no orçamento estadual ou municipal. Os principais instrumentos vigentes são:
O ProEquipaSUS é o programa do Ministério da Saúde voltado especificamente para o reequipamento de estabelecimentos de saúde da rede do SUS, com foco em equipamentos de diagnóstico e tratamento para atenção especializada e hospitalar. As transferências são condicionadas a plano de trabalho aprovado, CNES atualizado e comprovação de capacidade técnica de operação e manutenção.
O FIIS, Fundo de Incentivo à Inovação em Saúde operado pelo BNDES, financia investimentos em infraestrutura e equipamentos para entidades do setor de saúde, incluindo hospitais filantrópicos e Santas Casas, com condições diferenciadas de prazo e taxa de juros. Em 2025–2026, o FIIS destinou R$ 20 bilhões para o setor, com linha específica para equipamentos médicos.
Além desses mecanismos, o Ministério da Saúde opera sistemas de transferência fundo a fundo (Fundo Nacional de Saúde → Fundos Estaduais e Municipais) para equipamentos pactuados em planos de saúde regionais (PRS) dentro do âmbito da Programação Anual de Saúde.
Erros Mais Comuns nas Licitações de Equipamentos Hospitalares
A análise de licitações impugnadas e contratos problemáticos na área hospitalar revela um conjunto recorrente de erros evitáveis:
- ETP ausente ou superficial: especificar sem estudar, o erro mais frequente e com maior potencial de invalidação do processo pelo TCU ou CGU.
- Especificação com direcionamento de marca: inserir características que só um fabricante atende, mesmo que implicitamente, gera impugnações e pode anular o certame.
- Não verificar o registro ANVISA na habilitação: aceitar proposta de fornecedor com registro vencido ou com escopo diferente do equipamento ofertado.
- Ausência de requisitos de infraestrutura no edital: equipamento entregue sem que o ambiente esteja preparado, obra de adequação não prevista no orçamento da contratação.
- Prazo de entrega irreal: equipamentos de importação têm lead time de 90 a 180 dias, prazos de 30 dias geram inadimplemento contratual e multas.
- Aceite técnico sem testes instrumentais: assinar o aceite sem verificar os parâmetros técnicos, o equipamento pode estar fora de especificação e o hospital não terá instrumento legal para exigir correção.
- Contrato de manutenção não previsto: adquirir equipamento de alta complexidade sem orçar e licitar o contrato de manutenção, a garantia termina e o equipamento fica sem cobertura.
- Não exigir treinamento de manutenção: treinar apenas operadores clínicos e não os técnicos da engenharia clínica, dependência total do fabricante para manutenção preventiva.
O Papel do Portal Nacional de Contratações Públicas (PNCP)
O PNCP, Portal Nacional de Contratações Públicas é o repositório oficial centralizado de todas as contratações públicas brasileiras regidas pela Lei 14.133/2021. Para equipamentos hospitalares, o PNCP oferece funcionalidades relevantes tanto para compradores quanto para fornecedores:
- Pesquisa de preços: consulta de contratos celebrados por outros entes para o mesmo tipo de equipamento, base para estimativa de preço de referência no ETP.
- Atas de registro de preços: consulta e eventual adesão a atas de SRP vigentes de outros órgãos, o chamado "carona" de ata, com limites definidos na lei.
- Publicação obrigatória: editais, contratos, termos aditivos e atas de sessão pública devem ser publicados no PNCP, garantindo transparência e auditabilidade.
- Catálogo de itens: padronização de nomenclatura e especificações técnicas de itens recorrentes, reduz divergências entre compras do mesmo produto em entes diferentes.
Perguntas Frequentes
É possível exigir assistência técnica local no edital de equipamentos hospitalares?
Sim, desde que a exigência seja tecnicamente justificada no ETP e proporcional à complexidade e criticidade do equipamento. Para equipamentos críticos de alto custo, como ventiladores de UTI, monitores multiparamétricos ou equipamentos de diagnóstico por imagem, exigir que o fornecedor possua assistência técnica própria ou autorizada no estado ou região é juridicamente defensável e tecnicamente recomendável. A exigência deve estar no edital com critério claro de comprovação (atestado de autorização do fabricante, endereço do centro de serviço, comprovação de técnicos certificados), e não pode ser usada para restringir a competição sem fundamentação.
Qual a diferença entre registro e cadastramento na ANVISA para equipamentos médicos?
A RDC 751/2021 classifica produtos para saúde em quatro classes de risco (I a IV). Produtos de Classe I (menor risco) são submetidos a notificação; produtos de Classe II a cadastramento; e produtos de Classes III e IV a registro processo mais rigoroso com avaliação de dossiê técnico. Para fins de licitação, o edital deve exigir o tipo de anuência regulatória correspondente à classe do equipamento especificado, e a verificação deve ser feita no sistema de consultas da ANVISA com atenção ao status (ativo/vencido) e ao escopo da anuência.
O que é pré-qualificação e quando é aplicável em licitações de equipamentos médicos?
A pré-qualificação é um procedimento previsto na Lei 14.133/2021 pelo qual a administração seleciona previamente fornecedores ou produtos que atendem a requisitos técnicos definidos, criando uma lista de pré-qualificados da qual serão selecionados os participantes das licitações subsequentes. Para equipamentos hospitalares, é particularmente útil em contratos de fornecimento contínuo (como insumos laboratoriais) ou em aquisições recorrentes de equipamentos padronizados. A pré-qualificação agiliza o processo posterior e reduz o risco de habilitação de empresas sem capacidade técnica real.
Como tratar equipamentos de saúde que chegam sem manual em português?
A exigência de manual técnico em português deve constar do edital como requisito de entrega, e o não atendimento configura inadimplemento contratual, impedindo a emissão do aceite técnico definitivo. Caso o equipamento seja entregue sem manual em português, o hospital deve formalizar a notificação ao fornecedor com prazo definido para regularização, reter o pagamento da última parcela (se a estrutura do contrato assim permitir) e só emitir o aceite técnico após regularização. Além disso, a RDC 360/2020 da ANVISA estabelece obrigações de rotulagem e informações ao usuário em português para produtos para saúde, cujo descumprimento pode ser reportado à agência.
Hospitais privados também precisam licitar para comprar equipamentos médicos?
Não, a Lei 14.133/2021 e as obrigações licitatórias aplicam-se exclusivamente a entidades da administração pública direta e indireta. Hospitais privados, mesmo os filantrópicos conveniados ao SUS, adotam seus próprios processos de compra, que podem incluir cotações, concorrências internas ou processos de seleção de fornecedores regidos por regulamentos internos. No entanto, hospitais que recebem recursos federais (por emenda, convênio ou contrato de repasse) podem estar sujeitos a exigências específicas do agente financiador sobre processo de compra, o que deve ser verificado nas normas do programa de financiamento específico.
Para o profissional de engenharia clínica que deseja aprofundar sua atuação em gestão tecnológica, o domínio do processo de compra completa o ciclo da gestão do equipamento médico, desde a especificação e aquisição, passando pela manutenção ao longo da vida útil até a análise de obsolescência e substituição abordada no artigo sobre gestão do parque tecnológico hospitalar. Compreender o mercado de empresas de dispositivos médicos no Brasil também é essencial para fazer escolhas estratégicas fundamentadas no processo de compra.
Artigos relacionados
As 20 Maiores Empresas de Dispositivos Médicos no Brasil e Como Trabalhar Nelas [2026]
Ranking das 20 maiores empresas de dispositivos médicos no Brasil, multinacionais e nacionais, com dados de faturamento, localização, empregos e guia prático de carreira.
O Mercado de Dispositivos Médicos no Brasil: R$ 26 Bilhões em Dados e Análises [2026]
Análise do mercado de dispositivos médicos no Brasil com dados ABIMO, ABIMED e ABIIS: tamanho, segmentos, exportações, déficit comercial e projeções 2025-2030.
Mercado de Trabalho em Engenharia Biomédica: Dados, Tendências e Onde Buscar Vagas [2026]
Análise completa do mercado de trabalho em engenharia biomédica no Brasil: salários reais (CAGED), maiores empregadores, áreas em expansão (IA, robótica, SaMD), plataformas de vagas e comparativo global. Dados atualizados para 2026.
Quanto Ganha um Engenheiro Biomédico: Salários por Nível, Região e Especialidade [Dados CAGED 2026]
Salário engenheiro biomédico: R$ 8.658/mês em média (CAGED 2026), com teto de R$ 14.782 e piso legal de R$ 13.779. Dados por experiência, estado, setor e comparativo com outras engenharias.